Reporter Gene과 응용 분야
이 가이드는 bioluminescent reporter gene에 대한 개요를 제공하며, 적절한 reporter와 벡터 선택에 대한 가이드를 포함하고 있습니다. 본 페이지에서 소개된 reporter 벡터 및 세포주에 대한 주문 및 자세한 정보는 Reporter Gene Vectors 제품 페이지에서 확인하실 수 있습니다.
Reporter Gene 소개
Reporter gene이란 무엇인가?
Reporter gene은 발현 벡터에서 promoter 서열 또는 response element에 결합된 exogenous 코딩 영역으로, 세포의 특정 promoter 활성도를 측정할 수 있는 도구입니다. 일단 세포 내에서 발현되면, reporter 단백질 자체를 직접 측정하거나, 고유한 효소 활성을 분석하여, 결합된 promoter의 활성 정도를 정량적으로 평가할 수 있습니다. 이상적인 reporter gene은 관심 있는 세포 내에서 endogenous하게 발현되지 않아야 하며, 민감하고 정량적이며, 빠르고 간단하면서도 정확하고 재현 가능해야 합니다. 또한 안전하게 사용 가능한 특성을 지녀야 합니다.
Reporter gene의 역할은 무엇인가?
Reporter gene과 이와 관련한 검출 방법은 진핵생물의 유전자 발현과 조절 연구에 크게 기여해왔습니다. Reporter gene은 in vitro와 in vivo 모두의 다양한 응용분야에서 중요한 역할을 해 왔으며, 그 중에서도 세포 내 전사 활성의 지표로서 가장 많이 사용됩니다.
Reporter gene의 일반적인 활용 중 하나는 cis-작용 전사 조절 요소(cis-acting transcriptional element) 분석입니다. Reporter gene을 포함하는 plasmid인 reporter 벡터는 reporter 단백질 발현이 유전자의 전사 활성과 직접적으로 상응하기 때문에, promoter와 enhancer 요소의 기능을 확인하고 특성화하는 데 사용됩니다. 이러한 연구에서는 promoter, enhancer/silencer 서열을 reporter gene의 upstream 또는 downstream에 클로닝합니다. Promoter-reporter gene fusion 형태는 일반적인 형질 전환 방법을 통해 배양 세포에 도입하거나 생식세포에 삽입하여 형질전환 유기체를 생성할 수 있습니다. 이로써 reporter gene을 통해 세포, 조직, 발달 단계별 유전자 발현을 조절하는 promoter와 enhancer 요소를 규명할 수 있습니다.
trans-작용 인자(trans-acting factor)를 분석하기 위해서는 promoter-reporter gene fusion DNA를 관심 있는 trans-작용 단백질이나 RNA를 발현하는 다른 DNA 클론과 함께 동시에 형질전환 하거나, 샘플 처리를 통해 trans-작용 인자를 활성화시킵니다. 해당 단백질은 reporter gene의 upstream에 클로닝된 promoter 부위에 결합하는 transcription factor일 수도 있습니다. 예를 들어, HIV-1의 trans-작용 인자인 tat 단백질이 세포 내 도입된 다른 벡터에서 발현될 경우, reporter gene과 연결된 HIV-1 long-terminal repeat(LTR) 서열의 활성이 증가하고, 이로 인해 reporter gene 단백질 발현 또한 증가하게 됩니다.
또한, reporter는 promoter 활성 평가 외에도, untranslated region(UTR)이 mRNA 안정성에 미치는 영향, 단백질의 세포 내 위치 변화, translation 효율에 미치는 영향을 연구하는 데 널리 사용됩니다. 예를 들어, microRNA(miRNA) 결합 부위를 reporter gene의 downstream 또는 3´ 말단에 삽입하여 microRNA가 RNA 안정성에 미치는 영향을 연구할 수 있습니다.
Reporter gene의 활성은 어떻게 측정하는가?
Reporter gene 혹은 reporter gene 서열에서 translation된 단백질은 효소 활성, 분광광도학적 특성(spectrophotometric characteristics)을 검출하거나, 또는 항체 기반 분석법(antibody-based assay)을 통해 간접적으로 측정할 수 있습니다. 일반적으로 효소 기반 분석법은 소량의 reporter 효소만으로도 검출 가능한 수준의 반응 산물이 생성되기 때문에 더 민감합니다. 하지만 세포 내에 내인성(endogenous) 효소 활성이 존재하는 경우(예: β-galactosidase가 유당을 분해하는 경우), 높은 background가 발생할 수 있다는 한계가 있습니다. 항체 기반 분석법은 상대적으로 민감도가 낮지만, reporter 단백질이 효소 활성을 갖고 있는지 여부와 관계없이 reporter 단백질 자체를 검출할 수 있다는 장점이 있습니다.
궁극적으로 reporter assay는 단백질을 통해 bioluminescence 같은 관찰 가능한 지표를 이용하여 생물학적 결과를 측정하는 방법입니다.
Bioluminescent Reporter Gene
왜 형광보다 발광을 선택하는가?
광자(photon)는 주로 화학발광(chemiluminescence)과 형광(fluorescence)을 통해 생성되며, 이는 들뜬 상태의 분자 오비탈(excited-state orbital)에서 더 낮은 에너지 상태로 전이될 때 빛을 방출하는 원리입니다. 그러나 들뜬 상태가 형성되는 방식은 서로 다릅니다. 화학발광에서는 들뜬 상태가 발열성 화학 반응(exothermic chemical reaction)에 의해 만들어지는 반면 형광은 외부 빛의 흡수에 의해 들뜬 상태가 형성됩니다.
이러한 차이는 분석(assay)의 특성에 큰 영향을 줍니다. 예를 들어 형광 기반 assay은 강한 외부 빛을 사용해 들뜬 상태를 만들 수 있어 일반적으로 더 밝습니다. 반면, 발광 기반 분석에서는 화학 반응을 통해 광자를 방출하므로, 광자 방출이 상대적으로 낮습니다. 겉보기에는 형광의 더 밝아 분석의 민감도 향상과 직접적으로 연결될 것처럼 보이지만, 실제로는 그렇지 않은 경우가 많습니다. 분석 민감도는 signal-to-background 비율의 통계적 분석으로 결정되는데, 이는 샘플 측정 값에서 background 측정 값을 뺀 값으로 정의됩니다. 형광 분석은 background 신호가 높아, 상대 신호가 낮아지고 결과적으로 민감도는 떨어질 수 있습니다.
형광 분석에서 background 신호가 높은 주된 이유는, 형광 측정 장비(fluorometer)는 샘플로 유입되는 강한 여기광(photon)과 분석 대상 fluorophore에서 emission 되는 훨씬 적은 양의 광자를 완벽히 구별할 수 없기 때문입니다. 이러한 구별은 주로 방출되는 광자가 excitation photon보다 더 긴 파장을 가지는 특성을 이용한 광학 필터링(optical filtration)과 emission photon이 보통 excitation photon과는 다른 경로로 이동하는 광학적 기하학적 특성을 통해 이루어집니다. 그러나 광학 필터는 파장을 완벽히 구별할 수 없고, 광자는 산란(scattering)을 통해 방향이 바뀔 수 있습니다. 반대로 화학발광(chemiluminescence)은 들뜬 상태를 만들기 위해 외부 광원이 필요하지 않은 장점을 가집니다. 따라서 광자가 본질적인 background 신호를 형성하지 않아, 샘플에서 방출되는 광자(photon efflux)를 측정할 때 내재적 background 신호가 발생하지 않습니다. 그로 인해 발광 assay는 매우 낮은 background를 가지며, 아주 미세한 빛의 변화를 정밀하게 측정할 수 있습니다.
생물발광의 장점에 대해 더 알아보려면 이 기사를 참고하세요.
사용 가능한 발광 Reporter gene
생물발광(bioluminescence)은 살아 있는 생물이 스스로 빛을 내는 자연적 현상입니다. 발광의 기본 원리는 luciferase 효소와 발광 기질(luminogenic substrate, 예: luciferin)이 반응하여 빛을 생성하는 것입니다(Figure 1). 가장 널리 사용되는 luciferase는 딱정벌레(beetle) luciferase(예: firefly), Renilla luciferase, 그리고 심해 새우(deep sea shrimp) luciferase를 변형한 NanoLuc® luciferase입니다. Luciferase gene은 박테리아(bacteria), 딱정벌레(beetle, 예: 반딧불), Renilla, 심해 새우(Oplophorus), 해파리(Aequorea), Vargula, 와편모충류(Gonyaulax, dinoflagellate) 등 다양한 생물에서 발견되어 연구에 활용되고 있습니다. 이 중에서 박테리아, 딱정벌레, 심해 새우, Renilla 유래 luciferase만이 reporter gene으로 널리 사용되어 전사 발현(transcriptional expression)을 평가하는 데 활용되고 있습니다. 여기에서는 일반적으로 사용되는 luciferase reporter gene들을 소개합니다.
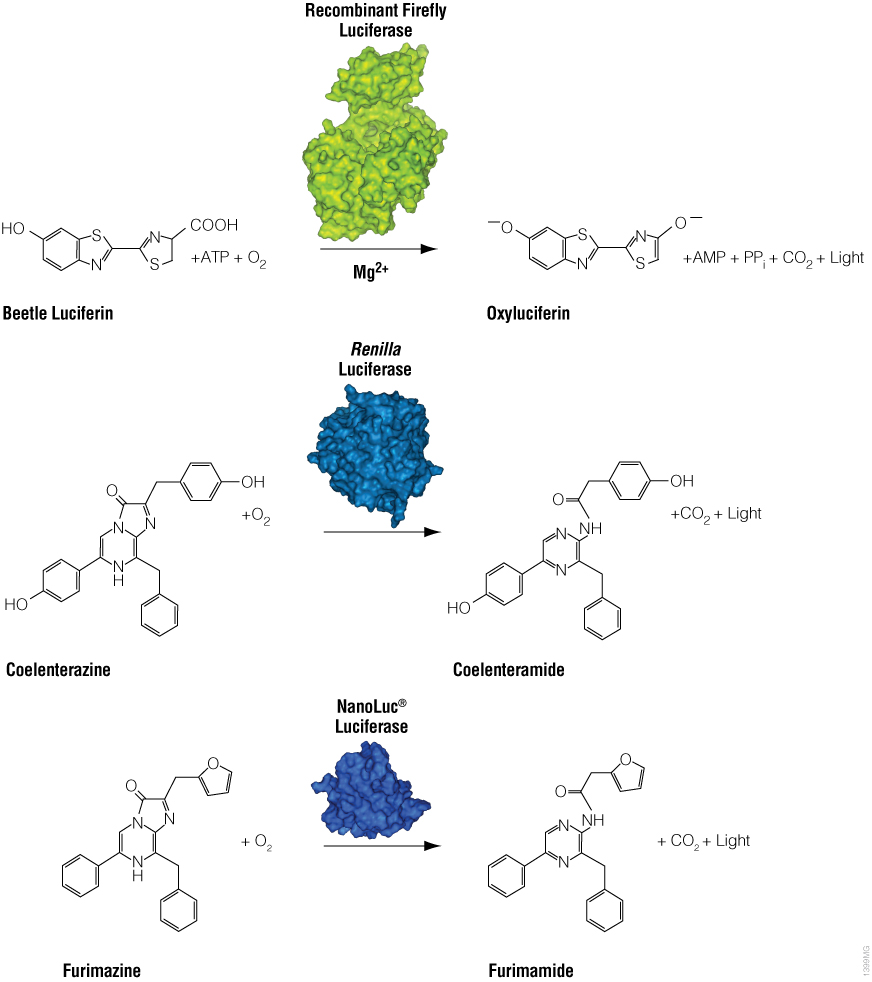
Figure 1. Firefly, Renilla, NanoLuc luciferase와 각기 다른 기질과 반응하여 빛을 생성하는 화학 반응의 도식도
Firefly Luciferase
Firefly luciferase는 가장 널리 사용되는 생물발광 reporter로, 약 61kDa 크기의 단량체(monomer) 효소입니다. 이는 북아메리카 반딧불이(Photinus pyralis)에서 유래되었으며 D-luciferin의 산화를 통해 녹색에서 노란색 빛(대략 550–570nm)을 방출하는 2단계 반응을 촉매합니다(Figure 1). 첫 번째 단계에서 luciferin은 ATP에 의해 활성화되어 luciferyl-adenylate와 pyrophosphate를 형성합니다. 두 번째 단계에서 luciferyl-adenylate는 산소 분자와 반응하여 전자적으로 들뜬 상태의 oxyluciferin과 CO2를 생성합니다. 들뜬 상태의 oxyluciferin이 기저 상태로 돌아오면서 빛을 방출합니다. 화학적 기질과 함께 사용할 경우, firefly luciferase는 초기에 강한 빛을 방출하고 약 15초 동안 급격히 감소한 뒤 낮은 수준의 지속적인 발광으로 이어집니다.
발광을 안정화하고 실험실에서 보다 편리하게 활용할 수 있도록 Coenzyme A(CoA)가 반응에 포함되며, 이는 수 분에 걸쳐 서서히 감소하는 최대 발광 강도를 제공합니다. CoA를 포함한 최적화된 분석법은 0.3초 미만의 시간 안에 안정적인 발광을 생성하며, 효소 농도의 1억 배 범위 이상 범위에서 선형성(linearity)을 보입니다. 또한 10–20 몰(moles) 이하의 효소도 정량할 수 있을 만큼 높은 민감도를 갖습니다.
Firefly luciferase가 reporter gene으로 널리 활용되는 이유는 효소 assay의 민감도와 편리성, 그리고 단백질 합성과 효소 활성이 긴밀히 연결되어 있기 때문입니다. luc 유전자가 코딩하는 firefly luciferase는 post-translational modification이 필요하지 않으며, mRNA가 번역되자마자 mature enzyme으로 기능합니다. 따라서 리보솜에서 방출되는 즉시 촉매 활성을 나타낼 수 있습니다. 또한, firefly luciferase는 다른 일반적인 reporter에 비해 세포 내 반감기가 상대적으로 짧습니다.
NanoLuc® Luciferase
NanoLuc® luciferase는 작은 크기의 단량체 효소(19.1kDa, 171 아미노산)로, 심해 새우 Oplophorus gracilirostris에서 유래된 luciferase를 기반으로 개발된 효소입니다(Hall et al, 2012). 이 유전공학적으로 개발된 효소는 새로운 기질인 furimazine을 사용하여, ATP 비의존적 반응을 통해 고강도의 blue-light 발광 (λmax = 465nm)을 생성합니다(Figure 1). NanoLuc®의 신호 반감기는 2시간 이상이며, 발광 강도는 firefly 또는 Renilla luciferase보다 약 100배 더 밝습니다(Figure 2). NanoLuc® luciferase의 높은 밝기가 왜 중요한지에 대해서는 아래 영상에서 확인할 수 있습니다:

포유류 세포에서 NanoLuc® luciferase는 post-translational modification, disulfide bond, 세포 내 구획화(subcellular partitioning)가 일어나지 않습니다. 이 효소는 넓은 pH 범위(pH 6–8)에서 활성을 유지하며, 높은 물리적 안정성을 보이고, 최대 55℃에서도 활성을 유지하고, 37℃ 배양 조건에서 15시간 이상 안정적으로 작동합니다.
다른 luciferase들과 달리, NanoLuc® luciferase는 표준 (lytic) reporter gene 분석과 secretion 기반 (nonlytic) reporter gene 분석 모두에 이상적입니다. 또한, 유전자의 크기(513bp)와 단백질 크기가 작아 reporter 바이러스에 도입하거나, 단백질 융합(fusion)에 매우 적합합니다. 더불어, live-cell 기질을 사용할 수 있어 이미징 분석에도 활용할 수 있습니다.
추가적으로, NanoLuc® luciferase 서열은 다른 유전자와 융합되어 융합 단백질(fusion protein)을 형성할 수 있습니다. 이렇게 형성된 융합 단백질은 세포 내에서 발현되어 다양한 응용에 활용될 수 있으며, 특히 BRET(Bioluminescence Resonance Energy Transfer)에서 발광 공여체(bioluminescent donor)로 사용될 수 있습니다.
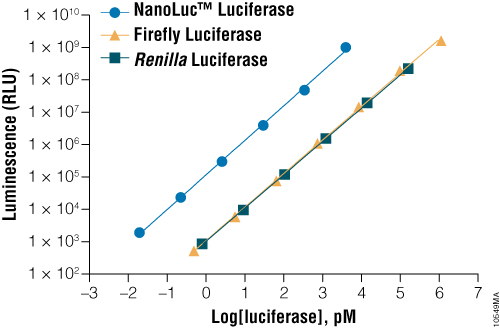
Figure 2. NanoLuc®, Firefly, Renilla luciferase assay의 민감도 비교
다양한 농도의 정제된 luciferase를 각 reporter 효소에 반응하는 검출 시약과 반응시킨 뒤 발광 signal을 측정했습니다. 동일한 농도에서 NanoLuc® luciferase는 firefly나 Renilla luciferase보다 약 100배 더 밝은 발광을 보였습니다. 발광 측정 시, NanoLuc® luciferase의 경우 Nano-Glo® Luciferase Assay, firefly luciferase의 경우 ONE-Glo™ Luciferase Assay System, Renilla luciferase의 경우 Renilla-Glo™ Luciferase Assay System을 사용하여 측정했습니다.
Renilla Luciferase
Renilla luciferase는 36kDa 크기의 단량체 효소로, coelenterazine을 산화시켜 coelenteramide와 480nm 파장의 청색 빛을 생성합니다(Figure 1). 숙주 생물인 Renilla reniformis(바다 팬지, 해산 산호류)는 물리적 자극을 받으면 밝은 green 섬광을 방출하여 포식자를 쫓아내는 것으로 알려져 있습니다. 이 green 빛은 luciferase와 GFP의 상호작용을 통해 생성되며, 이는 자연적인 BRET(bioluminescence resonance energy transfer)의 사례를 보여줍니다.
Reporter 분자로서 Rluc 유전자가 코딩하는 Renilla luciferase는 firefly luciferase와 유사한 장점을 제공합니다. 과거에는 auto-luminescence로 인해 높은 background 신호와 낮은 분석 민감도가 문제였으나, assay chemistry의 개선으로 이 문제는 거의 해결되었습니다. 또한, Renilla luciferase의 단순한 반응 메커니즘과 기질 개선으로, 오늘날에는 Renilla luciferase를 in situ나 in vivo 조건에서도 정량적으로 분석할 수 있게 되었습니다.
Reporter Gene 활성 최적화
이상적인 genetic reporter는 다음과 같은 특성을 가져야 합니다. i) 숙주 세포에서 균일하고 최적의 발현을 보일 것 ii) 분석에서 의도한 인자에만 반응하고 비정상적인 발현을 피할 것 iii) 내재적 안정성이 낮아 전사(dynamic transcriptional change)의 변화를 빠르게 반영할 것. 그러나 생물학적·효소학적 특성과 관계없이, 자연 상태의 luciferase는 반드시 최적의 유전적 reporter는 아닙니다. 이 때문에 Promega 과학자들은 luciferase 발현을 개선하여 불필요한 발현을 줄이고, 단백질의 반감기를 짧게 만들어 전사 변화가 빠르게 반영되도록 개량했습니다. 여기에서는 이러한 개선을 이루기 위한 핵심 전략을 설명합니다.
퍼옥시좀 표적화 신호 제거 (Removing the Peroxisomal Targeting Site)
일반적으로, 반딧불이의 발광 기관에서 luciferase는 광세포의 특수한 퍼옥시좀(peroxisome) 에 위치합니다. 그러나 firefly luciferase가 다른 세포에서 발현될 경우, C-말단 3개 아미노산(Ser-Lys-Leu)로 이루어진 보존된 전위 신호(translocation signal) 때문에 luciferase가 퍼옥시좀이나 글리옥시좀(glyoxysome)에 축적될 수 있습니다. 이는 정상적인 세포 생리와 유전적 reporter 성능에 영향을 줄 수 있습니다.
이를 해결하기 위해, Promega 연구진은 luciferase 유전자의 기존 C-말단 서열을 새로운 서열(-Ile-Ala-Val)로 대체하여 세포질형(cytoplasmic form) luciferase를 개발했습니다. 이 변형 luciferase는 NIH/3T3 cell에서 발현 시 기존 효소보다 4~5배 더 강한 발광을 안정적으로 보였습니다. 한편, Renilla 및 NanoLuc® luciferase는 이러한 표적화 서열이 존재하지 않아 퍼옥시좀 표적화의 영향을 받지 않습니다.
코돈 최적화 (Optimizing Codons)
유전 암호의 중복성 때문에 하나의 아미노산은 여러 코돈에 의해 코딩될 수 있지만, 생물 종마다 선호하는 코돈 사용 빈도는 다릅니다. 이 때문에 이종(non-native) 숙주 세포에서 단백질 translation 효율은 아미노산 서열은 그대로 유지하면서 코돈 사용 빈도를 조정하면 크게 향상될 수 있습니다. 그러나 반딧불이(firefly), 바다 팬지(sea pansy, Renilla reniformis), 심해 새우(deep sea shrimp)에서 유래된 원래의 luciferase 유전자는 포유류 세포에서 발현하기에 최적화되지 않은 코돈을 사용합니다. 따라서 Promega 연구진은 포유류 세포에서 선호되는 코돈으로 체계적으로 치환하는 동시에, 포유류 세포에서 부적절하거나 의도치 않게 작용할 수 있는 전사 조절 서열을 제거했습니다. 그 결과, luciferase의 발현 수준은 수십 배에서 많게는 수백 배까지 증가하였습니다(Figure 3 & 4).
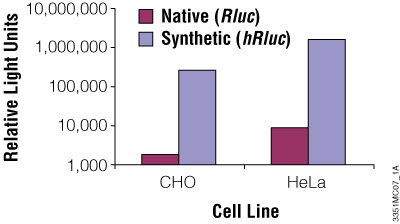
Figure 3. Synthetic Renilla luciferase 유전자는 포유류 세포에서 native 유전자보다 발현율이 높습니다. CHO cell과 HeLa cell에 synthetic hRluc 또는 native Rluc 유전자를 포함한 pGL3-Control Vector (Cat.# E1741; SV40 enhancer/promoter 포함)를 transfection하였습니다. Transfection 24시간 후 세포를 샘플링하여 Dual-Luciferase® Reporter Assay System을 사용해 Renilla luciferase 활성을 측정했습니다.
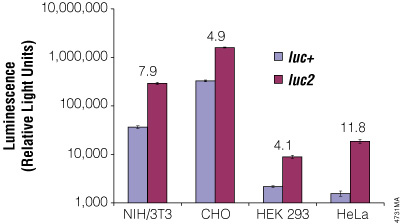
Figure 4. Firefly luc2 유전자는 luc+ 유전자보다 더 높은 발현율을 보입니다. luc2 유전자는 luc+ 유전자를 대체하여 pGL3-Control Vector에 클로닝하였으며, 두 개의 firefly luciferase 유전자는 동일한 pGL3-Control Vector backbone에 존재하게 되었습니다. 두 벡터는 transfection control인 phRL-TK Vector와 함께 NIH/3T3, CHO, HEK 293, HeLa cell에 co-transfection하였습니다. Transfection 24시간 후, 세포는 Passive Lysis 5X Buffer (Cat.# E1941)로 lysis 하였으며, Dual-Luciferase® Reporter Assay System (Cat.# E1910)을 사용해 발광 값을 측정하였습니다. 측정된 firefly luciferase 발광(RLU, relative light unit)은 phRL-TK Vector에서 측정된 Renilla luciferase 발현량을 기준으로 보정하였습니다. 각 세포주에서 luc+ 대비 luc2의 발현 증가(fold increase)는 각 그래프 막대 위에 표시하였습니다.
잠재적 전사 조절 서열 제거 (Removing Cryptic Regulatory Sequences)
Reporter gene 내의 잠재적 전사 조절 서열(cryptic regulatory sequence)은 전사 과정에 부정적인 영향을 주어, reporter의 비정상적인 발현을 초래할 수 있습니다. 이러한 잠재적 서열은 전사인자 결합 부위이거나, 또는 promoter 모듈(최소 두 개의 전사인자 결합 부위가 스페이서에 의해 분리된 구조; Klingenhoff et al., 1999)일 수 있습니다. 또한, enhancer elemen는 promoter 서열이 없어도 전사 수준을 증가시키거나, 전사 조절 서열이 있을 경우 기초적인 유전자 발현 수준을 높일 수 있습니다. 이처럼 이러한 조절 서열들은 전사를 증가시키거나 감소시켜, 결과적으로 유전자 발현 전반에 영향을 미칩니다(Klingenhoff et al., 1999).
luc 유전자 내의 이러한 잠재적 전사 조절 서열은 아미노산 서열을 변경하지 않고 제거하여 luc2 유전자가 만들어졌습니다. 추가적으로, 스플라이싱 부위(splice site), poly(A) 추가 서열, Kozak 서열(포유류 세포의 번역 시작 부위), E. coli promoter 서열, E. coli 리보솜 결합 부위와 유사한 서열도 가능한 범위 내에서 제거하였습니다. 이 과정을 통해 잠재적 전사 조절 서열의 수가 크게 줄어들었으며(Figure 5), 비정상적인 전사가 일어날 위험 또한 낮아졌습니다. 비슷한 접근 방식이 Renilla luciferase에도 적용되어 hRluc 유전자가 만들어졌습니다.
Figure 5. luc2 유전자에서 감소된 전사 인자 결합 부위 수
luc+ 유전자에서 확인된 전사 인자 결합 부위(consensus transcription factor-binding site)의 수는 luc2 유전자에서 크게 감소되었습니다.
분해 신호(Degradation Signal) 추가
Reporter 분석에서 측정되는 것은 세포 내에 축적된 전체 reporter 단백질 양입니다. 이러한 축적은 reporter 단백질의 세포 내 반감기, 즉 단백질과 mRNA의 안정성에 의해 결정됩니다. 더 역동적인 reporter일수록 upregulation과 downregulation 모두에 따른 전사 변화를 더 잘 반영할 수 있습니다.
NanoLuc® luciferase는 firefly 및 Renilla luciferase보다 안정적입니다. 그러나 단백질의 안정성이 높은 만큼 reporter의 반응은 실제 전사 변화보다 몇 시간 지연될 수 있습니다. 이를 개선하기 위해 Promega 연구진은 luciferase reporter gene에 단백질 분해 서열(protein degradation sequence)을 융합하여 불안정화된(destabilized) luciferase reporter를 개발했습니다(Li et al., 1998). 다양한 분해 서열의 반응 속도 및 신호 강도에 대한 효과를 평가한 후, Promega 연구진은 두 가지 서열인 PEST 단백질 분해 서열과 CL1과 PEST 두 가지 분해 서열 조합을 선택했습니다. 이를 통해 생성된 luc2P (PEST 서열 포함)와 luc2CP (CL1+PEST 서열 포함)는 Rapid Response™ 유전자로 명명되었으며, 더 빠르게 자극에 반응하지만 신호 강도는 감소합니다. luc2P는 약 1시간의 단백질 반감기(세포주 별로 차이 있음)를 가지고 luc2 (약 3시간 반감기)보다 훨씬 빠르게 반응하며, 중간 수준의 신호 강도를 유지합니다. luc2CP는 약 0.4시간의 반감기를 가지며 가장 빠르게 반응하지만 신호 강도가 가장 낮습니다. NanoLuc®-PEST (NlucP)은 단백질 반감기 약 20분이나 효소의 높은 특이적 활성(specific activity) 덕분에 여전히 밝은 신호 유지합니다. 이러한 destabilized reporter는 더 빠르게 반응하고, 종종 안정화된 reporter보다 더 높은 signal-to-background 비율을 보여줍니다.
분비 신호(Secretion Signal) 추가
원래 Oplophorus luciferase는 기질 coelenterazine을 산화시켜 blue 빛을 발생시키며, 이는 새우가 포식자를 방어하기 위해 분비하는 메커니즘입니다. 실험실 환경에서는, 분비성 reporter가 세포 용해(cell lysis) 없이 세포 생존을 유지한 채로 세포 외부에서 신호를 검출할 수 있어 유용합니다. 포유류 세포에서 단백질 분비 효율을 극대화하기 위해, Promega 연구진은 원래의 분비 신호를 포유류 단백질 분비 신호로 교체하였으며, 이로써 secNluc 유전자를 개발했습니다. 분비성 NanoLuc® luciferase는 효소의 열안정성(thermostability) 덕분에 세포외 배지에 축적될 수 있어, 세포를 손상시키지 않는(nondestructive) reporter gene 분석에 이상적입니다.
Reporter Gene 벡터
벡터는 reporter gene 서열을 배양 세포에 도입하기 위해 사용하는 plasmid(염색체 외 요소)입니다. 벡터는 단순히 reporter gene을 제공할 뿐만 아니라, MCS, promoter, response element, poly(A) 서열, 포유류 selectable marker, 그 외 발현 및 선택에 도움을 주는 다양한 서열 요소들을 포함할 수 있습니다. 따라서 reporter 벡터는 reporter assay의 성공을 위해 필수적입니다.
Firefly와 Renilla luciferase를 코딩하는 pGL4 Luciferase Reporter 벡터
벡터는 reporter gene을 숙주 세포에 전달하는 역할을 하기 때문에, 벡터 backbone에 존재하는 전사인자 결합 부위나 promoter 모듈 같은 조절 서열은 높은 background 신호나 비정상적 반응을 유발할 수 있습니다. 이러한 문제는 pGL3 luciferase reporter 벡터를 포함한 포유류 reporter 벡터에서 흔히 발생합니다. Promega 연구진은 앞서 reporter gene에서 적용한 cleaning 전략을 벡터 전체에 확장하여, reporter 기능을 유지하면서 가능한 모든 잠재적 조절 서열을 제거했습니다. 추가적으로 MCS 부위에는 관심 있는 DNA 서열을 쉽게 삽입할 수 있도록 고유한 SfiI 제한효소 절단 부위로 재설계하였고, f1 origin of replication은 제거하였으며, 인트론(intron)도 하나 삭제하였습니다. 또한, 합성 poly(A) 신호/전사 정지 서열을 MCS 영역의 upstream (promoter가 없는 벡터), 또는 HSV-TK, CMV, SV40 promoter의 upstream (promoter가 포함된 벡터)에 위치하도록 설계하였습니다. 이러한 광범위한 개량 작업을 통해 완전히 새롭게 설계된 pGL4 벡터 backbone이 탄생했습니다. 또한, 강력한 CMV promoter를 부분적으로 제거하여 보다 세밀한 조절이 가능한 CMV promoter변형 버전의 pGL4 벡터 시리즈도 개발되었습니다.
pGL4 luciferase 벡터 패밀리는 다양한 특징의 벡터를 제공합니다. 여기에는 최적화된 firefly 또는 Renilla luciferase gene 선택, 시간적 반응성을 개선한 Rapid Response™ 버전, mammalian selectable marker, promote가 없는 기본 벡터, promoter가 포함한 대조(control) 벡터, 그리고 여러 가지 response element를 선택할 수 있는 미리 설계된 벡터 등이 포함됩니다(Figure 6).

Figure 6. pGL4 luciferase reporter 벡터 패밀리는 다양한 추가 기능을 제공합니다. 여기에 luciferase gene 선택, Rapid Response™ 버전, 다양한 mammalian selectable marker, 그리고 promoter 및 response element의 유무에 따른 벡터 등이 포함됩니다.
NanoLuc® luciferase를 코딩하는 pNL 벡터
NanoLuc® luciferase는 전사 조절 reporter 유전자 분석에 사용하기 위해 다양한 벡터로 제공됩니다. 이러한 pNL 벡터는 pGL4 벡터 backbone을 기반으로 하며, 따라서 여러 동일한 장점을 제공합니다: 전사인자 결합 부위와 기타 잠재적 조절 서열 제거를 통해 비정상적 결과의 위험을 줄이고, 기존 plasmid로부터의 서열 transfer가 용이하며, 여러 promoter(no promoter, minimal promoter, viral promoter 등) 중 선택이 가능합니다. 이 벡터 패밀리는 unfused Nluc, PEST-불안정화형 NlucP, 분비형 secNluc과 같은 NanoLuc® 유전자의 선택을 제공합니다. 이러한 NanoLuc® 유전자 변형체는 코돈 최적화되어 있으며, 잠재적 조절 서열이나 일반적인 제한효소 절단 부위와 같은 바람직하지 않은 특징들이 제거되었습니다.
또한, 단일 전사체에서 NanoLuc®과 firefly luciferase를 모두 발현하는 coincidence reporter 벡터도 있습니다. 이러한 벡터는 no promoter, minimal promoter 또는 CMV promoter를 갖춘 형태로 제공되어 고처리량 스크리닝(high-throughput screening)에 사용할 수 있습니다. Reporter 벡터를 사용하여 세포 스트레스 반응에 관여하는 두 가지 주요 신호 단백질의 turnover 속도를 연구할 수 있습니다.
Reporter 벡터
프로메가의 광범위한 최첨단 bioluminescent reporter 벡터 라인에는 pGL4 벡터(최신 세대 firefly 및 Renilla luciferase reporter 벡터)와 NanoLuc® luciferase reporter 유전자를 포함하는 pNL 벡터가 포함됩니다.
Reporter gene 활성 측정
생물발광 기반 검출 분석의 원리는 효소와 기질 간의 효율적인 빛 방출 화학 반응을 분석에 활용하는 것입니다. 연구 중인 과정과 관련하여 하나의 성분만 변하게 하고 나머지 반응 성분의 농도는 일정하게 유지하면, 생성되는 빛은 그 변하는 성분의 농도에 직접적으로 비례하게 됩니다. 즉, 관찰 가능한 지표를 반응 결과와 연결하는 것입니다. Luciferase를 사용하는 assay에서는 이 변화하는 성분이 luciferase 자체이거나, 그 기질 혹은 보조인자(cofactor)가 될 수 있습니다. 생물발광은 background 신호가 매우 낮기 때문에, 비례 관계의 직선 범위(linear range)가 매우 넓어 보통 변화하는 성분 농도의 104–108배 농도 범위까지 확장될 수 있습니다.
세포 내 luciferase는 일반적으로 세포를 용해하는 detergent가 포함된 buffer를 첨가해 세포를 파괴하고, luciferase 기질을 넣어 발광 반응을 유도함으로써 정량합니다. 이때 발광은 시간이 지나면서 점차 감소합니다. Firefly 및 Renilla luciferase assay에서 수 분에서 수 시간까지 안정적인 발광을 유지하려면 발광 반응을 일정 정도 억제해야 합니다. 이러한 조건에서도 샘플당 10–20 몰 수준 이하의 luciferase까지 정량할 수 있으며, 이는 세포당 약 10분자 정도에 해당합니다.
대조적으로, NanoLuc® luciferase는 본래 신호 반감기가 더 길게 유지됩니다. NanoLuc® luciferase 활성을 측정하기 위해 새로운 기질인 furimazine을 사용하는 NanoLuc® 기반 assay는 훨씬 더 밝은 신호를 나타내며, 발광 감소 속도가 매우 느려 신호 반감기가 약 120분에 이릅니다. 이러한 긴 반감기 assay는 reporter gene을 다양한 분야에 응용하는 데 매우 편리합니다. 단순히 시약을 첨가하고, 그 결과 발생하는 발광을 측정하면 됩니다.
대부분의 reporter gene assay는 하나 또는 두 개의 reporter gene을 사용합니다. 가장 흔히 두 번째 reporter는 대개"대조(control)” 벡터에서 발현되며, 이는 실험용 reporter의 결과를 보정(normalization)하는 데 사용됩니다. 예를 들어, 두 번째 reporter는 세포 개수나 transfection 효율 차이를 보정할 수 있습니다. 일반적으로 대조 reporter gene은 constitutive promoter에 의해 발현되며, control 벡터는 ”실험용” 벡터와 함께 co-transfection 합니다. 두 reporter 산물의 상대적 활성을 개별적으로 측정할 수 있도록, 실험 벡터와 대조 벡터에는 서로 다른 reporter gene이 사용됩니다. 아래의 Introduction to Reporter Gene Assays 애니메이션은 Dual-Luciferase® Reporter Assay System을 활용하여 promoter 구조, 유전자 조절 및 신호 전달 경로를 연구하는 reporter assay의 기본 디자인을 보여줍니다.

또는, 두 개의 reporter gene을 모두 실험용 reporter로 사용하는 dual-reporter assay로 디자인할 수도 있습니다. 이러한 dual-reporter assay는 하나의 실험에서 더 많은 정보를 효율적으로 얻는 데 특히 유용합니다. Dual-Luciferase assay에서 하나 또는 두 개의 실험용 reporter를 사용하는 방법에 대한 더 자세한 내용은 NanoDLR™ Dual Reporter Assay 형식을 선택하는 방법에 관한 글을 참고하세요.
다음 섹션에서는 연구 목적에 맞는 reporter gene과 assay를 선택하는 데 도움이 되는, 특정 bioluminescent reporter assay에 대한 정보를 제공합니다. Table 1, 2 and 3에는 사용 가능한 luciferase gene, assay, 시약들이 요약되어 있습니다.
Single Reporter Assay
단일 reporter에 기반한 분석은 세포에서 유전자 발현 데이터를 얻는 가장 신속한 방법입니다. 그러나 세포는 본질적으로 복잡하기 때문에, 단일 reporter 분석으로 얻은 정보만으로는 상세하고 정확한 결과를 얻기에 충분하지 않을 수 있습니다. 따라서 reporter assay 방법을 선택할 때 가장 먼저 고려해야 할 점 중 하나는, 단일 reporter로 얻은 정보가 충분한지, 아니면 두 번째 reporter에서 얻을 수 있는 추가 정보(예: transfection 효율이나 세포 수 차이의 보정)가 필요한지 여부입니다. 더 많은 정보가 필요하다면 아래의 Dual-Reporter Assays 섹션을 참고하세요.
Luciferase assay를 선택할 때는 발광 강도(luminescence intensity)와 신호 지속 시간(duration) 사이에서 균형을 맞춰야 하는 경우가 많습니다. 강한 발광 반응은 상대적으로 빨리 소멸하는 경향이 있기 때문입니다. Firefly 또는 Renilla luciferase assay를 사용하여 최대 발광을 얻으면 높은 민감도를 제공하지만, 신호 반감기가 더 길고 발광이 더 안정적인 분석법은 multi-well plate에서 실험을 수행할 때 더 편리합니다. 신호 반감기가 연장된 firefly luciferase assay으로는 ONE-Glo™ Luciferase Assay System (Cat.# E6110)과 ONE-Glo™ EX Luciferase Assay System (Cat.# E8110)이 있습니다. ONE-Glo™ Luciferase Assay System은 최대 발광 강도를 제공하며, 신호 반감기가 약 45분이고, 최적화 되지 않은 반응 조건(non-optimal condition)에서도 안정적입니다. ONE-Glo™ EX Reagent는 신호 반감기가 더 길고(약 2시간), buffer에 넣어 만든 reagent는 4℃ 또는 상온에서도 보다 안정적이며, 세포 배양 배지에 포함된 phenol red의 간섭을 덜 받으며, 다른 luciferase assay reagent보다 냄새가 적습니다.
Figure 7. 다양한 firefly luciferase assay에서 발광 신호 안정성을 보여주는 데이터 예시
이 실험에서 정제된 firefly luciferase(13.8ng/ml) 100µl를 96-well plate에 분주한 뒤, 각각 Bright-Glo™, ONE-Glo™, ONE-Glo™ EX, Dual-Glo® Luciferase, Steady-Glo® reagent 100µl와 혼합했습니다. 발광은 2시간 동안 주기적으로 측정되었습니다(n = 8).
Steady-Glo® Luciferase Assay System은 발광 지속 시간이 더 길지만, 발광 강도는 낮습니다. Steady-Glo® Reagent는 세포 배양 배지에 직접 첨가되므로, 세포 용해 과정이 별도로 필요하지 않습니다. 이를 통해 multi-well plate에서 세포를 배양한 뒤, 단일 단계로 reporter 발현을 측정할 수 있습니다. 또한, 신호 강도와 반감기가 서로 다른 Renilla luciferase assay도 이용할 수 있습니다.
발광 강도를 낮추고 신호 반감기를 늘려야 하는 문제는 NanoLuc® luciferase에서는 고려하지 않아도 됩니다. Nano-Glo® Luciferase Assay System (Cat.# N1110)은 단순한 단일 첨가(single-addition) 시약으로, 일반적인 조직 배양 배지에서 약 120분의 신호 반감기를 가지는 glow-type 신호를 생성합니다. 이 시약은 NanoLuc® luciferase를 발현하는 세포에 직접 사용할 수 있는 lysis buffer을 포함하고 있으며, 분비성 luciferase가 포함된 배지에서도 호환됩니다.
Dual-Reporter Assays
하나의 분석에서 두 개의 reporter를 측정하는 것을 dual-reporter assay라고 하며, 두 reporter가 모두 luciferase일 경우 이를 dual-luciferase assay라고 합니다. 가장 일반적으로 사용되는 dual-reporter assay는 firefly와 Renilla luciferase 활성을 모두 측정하는 것이지만, 차세대 dual luciferase assay은 NanoLuc과 firefly luciferase를 사용합니다. 이러한 luciferase 쌍은 서로 다른 기질을 사용하기 때문에 효소 특이성으로 구별될 수 있습니다. 대부분의 dual- luciferase assay는 각 샘플에 두 가지 시약을 순차적으로 첨가하고, 첨가 후 발광을 측정하는 방식으로 수행됩니다. 첫 번째 시약을 첨가하면 첫 번째 luciferase reporter 반응이 활성화되고, 두 번째 시약을 첨가하면 첫 번째 luciferase 활성이 소멸되며 동시에 두 번째 luciferase 반응이 시작됩니다.
Nano-Glo® Dual-Luciferase® Reporter Assay System은 firefly와 NanoLuc® luciferase 활성을 측정합니다. 이 조합은 여러 가지 장점을 가지는데, 그 중에는 firefly luciferase 활성이 더 효과적으로 제거(quenching)되어 낮은 background 신호를 제공한다는 점과, NanoLuc®의 더 밝은 발광으로 인한 높은 민감도가 포함됩니다. 또한, 긴 신호 반감기(firefly와 NanoLuc® 모두 약 2시간)가 있어 고처리량(high-throughput) 스크리닝에 특히 유용합니다. 낮은 firefly background과 밝은 NanoLuc® 신호는 assay 구성을 더 유연하게 할 수 있도록 해주며, NanoLuc® 또는 firefly 중 어느 것이든 실험용 reporter로 사용할 수 있고, 나머지는 normalization control로 사용할 수 있습니다. 또는 두 reporter gene을 모두 실험용 reporter로 사용하여, 하나의 assay 세트에서 더 많은 정보를 얻을 수도 있습니다.
기존 기술인 Dual-Luciferase® Reporter Assay System (Cat.# E1910)은 하나의 샘플에서 firefly와 Renilla luciferase 활성을 순차적으로 측정합니다. 이 시스템은 assay을 수행하기 전 세포 lysis가 필요하며, multi-well plate에서 사용 시 시약 injector가 필요합니다.
Dual-Glo® Luciferase Assay System역시 하나의 샘플에서 firefly와 Renilla luciferase 활성을 측정하며, 더 긴 luciferase 신호 반감기를 제공합니다. 이는 multi-well plate에서 reporter assay을 수행할 때 특히 유용합니다. 다른 multi-well plate 전용 시약과 마찬가지로, Dual-Glo® Assay는 세포 lysis 과정 없이 포유류 세포 배양 배지에서 직접 작동합니다.
일반적으로, dual reporter assay는 실험의 정확성과 효율성을 향상시키는데, 그 이유는 i) 의미 있는 상관관계를 가릴 수 있는 변동성을 줄이고, ii) 실험 시스템에 내재할 수 있는 방해 현상을 보정하며, iii) 샘플 간 transfection 효율 차이를 보정할 수 있기 때문입니다. 또한, dual reporter assay는 고처리량 스크리닝에서 reporter 단백질과 화합물의 직접적 상호작용으로 인한 비특이적 결과(예. “false” hit)의 수를 줄여줄 수 있습니다. 서로 다른 화합물 간섭 특성을 가진 co-incidence reporter를 사용하면, 관심 있는 생물학적 경로를 조절하는 화합물과 reporter 효소의 안정성이나 활성을 변화시키는 화합물을 구별하는 데 도움이 됩니다.
Reducing Variability
세포는 매우 복잡한 미세 환경을 갖고 있어, 동일한 실험 내 샘플 간 혹은 서로 다른 시점에 수행된 실험 간에 상당한 변동성이 발생할 수 있습니다. 이러한 어려움에는 샘플 간 균일한 세포 밀도와 생존력을 유지하는 것, 그리고 외래 DNA에 의한 형질전환을 재현성 있게 수행하는 것이 포함됩니다. Multi-well plate를 사용할 경우, plate 전체에서 열 분포와 습도의 차이로 인해 발생하는 edge effect 같은 변수가 추가로 발생합니다. Dual-reporter assay는 이러한 변동성을 상당 부분 보정할 수 있어, 샘플 간 비교를 더 정확하고 의미 있게 만들어 줍니다(Hawkins et al., 2002; Hannah et al., 1998; Wood, 1998; Faridi et al., 2003).
Live-Cell Substrates
연구자들은 세포에 미치는 영향을 최소화하면서 세포 활동을 모니터링하길 원합니다. 대부분의 reporter 활성 분석은 세포를 파괴하여 reporter 효소가 위치한 환경을 정밀하게 제어하는 endpoint 방식을 사용합니다. 그러나 nonlytic assay를 사용해 reporter gene 활성을 측정하는 것에는 장점이 있습니다. 여기에는 시간에 따른 발현 변화를 지속적으로 추적할 수 있다는 점과, cell health를 평가하는 다른 분석법과 multiplexing 할 수 있다는 점이 포함됩니다. Promega 연구진은 세포를 파괴하지 않고 luciferase 활성을 모니터링할 수 있는 다양한 live-cell substrate를 개발했습니다.
배양 배지에 단일 시약만 첨가하면, NanoLuc® luciferase 활성을 수 시간에서 길게는 며칠 동안 모니터링할 수 있습니다. Nano-Glo® Live Cell Assay System은 최대 광도를 제공하며 약 2시간까지 reporter 활성을 모니터링할 수 있습니다. Nano-Glo® Vivazine® Live Cell Substrate는 빛 강도는 감소하지만 수 시간 동안 NanoLuc® 활성을 모니터링할 수 있습니다. Nano-Glo® Endurazine™ Live Cell Substrate는 신호 강도는 가장 낮지만, 신호 안정성이 가장 높아 며칠 동안 reporter 활성을 모니터링할 수 있습니다. 이러한 live-cell 검출 시약은 reporter 발현에 대한 동역학적(kinetic) 측정을 가능하게 하여, 단백질 상호작용 연구와 time course 연구를 단순화할 수 있습니다.
Renilla luciferase 는 산소와 coelenterazine 만으로 발광을 생성하므로, 살아 있는 세포에서 발광을 측정하는 간단한 luciferase 시스템을 제공합니다. EnduRen™ 및 ViviRen™ Live Cell Substrate는 수용액에서 coelenterazine의 불안정을 극복하여, Renilla luciferase를 발현하는 살아 있는 세포에서 쉽게 발광을 측정할 수 있습니다. 세포가 살아 있기 때문에, 이를 다른 분석법과 multiplexing하여 생존 세포 수를 동시에 측정할 수도 있습니다.
Live-cell substrate의 대안으로는 분비형 reporter 단백질이 있습니다. 이는 세포 배양 배지에서 reporter 활성을 측정하여 정량화할 수 있습니다. 예를 들어, NanoLuc® luciferase에 N-말단 분비 신호를 융합한 secNluc은 reporter assay 전이나 assay 중에 세포 lysis 과정이 필요하지 않습니다.
Reporter Assay 리소스
- Single-Reporter Assays:
NanoLuc® Luciferase와 GloMax® Discover System을 사용하여 생리학적 수준에서 HIF1α 발현 검출 - Dual-Reporter Assays:
Luciferase reporter assay 선택하기: 비교 가이드
생물발광 reporter assay 설계: 실험 reporter 선택하기
생물발광 reporter assay 설계: 보정(Normalization)
NanoDLR™ Dual-Luciferase Assay System을 사용하여 primary reporter와 control reporter를 혼합하여 활용하기
Reporter Assay 제품
Promega reporter assay 제품은 single reporter 또는 dual reporter 형식에서 폭넓은 선택지를 제공합니다.
Reporter Gene의 응용
Reporter gene의 전통적인 사용은 주로 유전자 발현을 분석하고, promoter와 enhancer 같은 cis-작용 유전 요소(cis-acting genetic element)의 기능을 규명하는 데 있습니다(이른바 “promoter bashing”). 일반적인 실험에서는 promoter 영역에 결실(deletion)이나 돌연변이(mutation)를 도입한 후, 이들이 reporter gene의 발현에 미치는 영향을 정량할 수 있습니다. 그러나 reporter gene은 유전자 발현과 직접적으로 관련되지 않은 세포 과정도 연구하는 데 사용할 수 있습니다. 예를 들어, cell health나 신호 전달 경로(signaling pathway) 같은 과정을 연구하는 데도 활용됩니다. 자세한 내용은 Introduction to Bioluminescent Assays 애니메이션에서 확인하실 수 있습니다.

세포 생리학적 변화에 대한 보정(normalization)
세포 생리와 관련된 다양한 현상은 reporter gene 발현에 영향을 줄 수 있습니다. 특히 문제가 되는 부분은 세포 독성(cytotoxicity)의 영향으로, 이는 single reporter assay에서 실제 유전자 발현 감소와 유사한 결과를 나타낼 수 있습니다. 따라서 reporter assay를 cell viability assay이나 cytotoxicity assay와 함께 multiplexing하여 reporter 발현과 세포 생존을 독립적으로 동시에 모니터링하면 데이터 해석 오류를 줄일 수 있습니다 (Farfan et al., 2004). Multiplexing assay를 사용하면 RNAi에 의한 표적 억제(target suppression)와 같은 세포 내 이벤트가 세포 생리학적 변화에 어떤 결과를 미치는지 연관 지어 해석할 수 있습니다 (Hirose et al., 2002).
CellTiter-Glo® 2.0 Cell Viability Assay (Cat.# G9241)와 CytoTox-Glo™ Cytotoxicity Assay (Cat.# G9290) 같은 발광 기반 세포 생존력 또는 세포 독성 분석법은 안정화된 firefly luciferase를 이용하여 cell health 상태를 반영하는 발광 신호를 생성합니다. 이러한 분석법들은 firefly luciferase를 포함하고 있기 때문에 firefly luciferase reporter assay와는 같이 사용할 수 없습니다. 하지만 non-destructive luciferase assay와는 쉽게 multiplexing이 가능합니다. 예를 들어, 배양액에 Nano-Glo® Live Cell Substrate를 첨가해 NanoLuc® luciferase 발현을 측정합니다. Reporter 측정이 끝난 후에는 CellTiter-Glo® 2.0 또는 CytoTox-Glo™ reagent를 첨가하여 NanoLuc® luciferase를 불활성화시키고 발광을 발생시켜 cell viability를 평가할 수 있습니다. 혹은 배양 배지 일부를 사용해 Nano-Glo® Luciferase Assay System으로 분비된 NanoLuc® reporter의 활성을 정량할 수도 있습니다. 또는 발광 기반 reporter assay를 형광 기반 cell viability 및 cytotoxicity assay와 multiplexing하여 cell health를 모니터링하고 single reporter assay 결과를 보정(normalization)할 수 있습니다. 예를 들어, CellTiter-Fluor™ Cell Viability Assay (Cat.# G6080)는 non-lytic 형광 분석법으로, 세포 집단 내 살아있는 세포 수를 상대적으로 측정할 수 있습니다. CellTox™ Green Cytotoxicity Assay (Cat.# G8741)는 살아 있는 세포에서는 배제되고, 죽은 세포의 DNA에 선택적으로 결합하는 dye를 사용합니다. 이 dye는 DNA와 결합하면 형광이 크게 증가하며, 그 결과 형광 강도는 세포 독성 수준에 비례합니다. 이러한 cell health assay는 Bright-Glo™, Steady-Glo®, ONE-Glo™ Luciferase Assay System, Renilla-Glo® Luciferase Assay System, Nano-Glo® Live Cell Substrate와 같은 homogenous luciferase assay reagen와 multiplexing 하기에 적합합니다 (Zakowicz et al., 2008).Reporter Assay 및 Cell Health에 대한 추가 자료
RNA Interference 모니터링
RNA interference (RNAi)는 표적 mRNA와 상보적인 이중가닥 RNA(double-stranded RNA)가 표적 mRNA 분해를 유도하여 유전자를 특이적으로 억제하는 현상입니다. 이러한 RNAi, 또는 더 일반적으로는 RNA silencing 현상은 유전자 기능을 분석하는 강력한 도구로 자리잡았습니다.
생물발광 reporter는 RNAi 연구에도 활용되고 있습니다. 예를 들어, pmirGLO Dual-Luciferase miRNA Target Expression Vector (Cat.# E1330)는 dual-luciferase 기술을 기반으로 하며, firefly luciferase는 mRNA 조절을 모니터링하는 주요 reporter로, Renilla luciferase는 normalization을 위한 control reporter로 사용됩니다. pmirGLO vector는 firefly luciferase 유전자의 downstream 또는 3´ 말단에 miRNA 타겟 사이트를 삽입하여 miRNA 활성을 정량적으로 평가할 수 있습니다. Firefly luciferase 발현이 감소하면, 내인성 또는 도입된 miRNA가 클로닝된 miRNA 표적 서열에 결합함을 의미합니다.
세포 신호전달 경로 분석
Luciferase reporter assay는 세포 신호전달 경로를 연구하는 데 널리 사용되며, 신약 개발을 위한 high-throughput 스크리닝 도구로도 활용됩니다(Brasier et al., 1992; Zhuang et al., 2006). Reporter gene 발현을 조절하는 regulatory element를 클로닝한 합성 벡터를 이용하면 신호전달을 모니터링하고, 관여하는 신호전달 경로를 규명할 수 있습니다. Luciferase 유전자를 reporter 벡터 내 특정 response element(RE)에 연결하고, 이 construct를 세포에 transfection한 뒤 특정 처리를 가하고 reporter 활성을 측정함으로써, 어떤 RE가 활성화되는지, 따라서 어떤 신호전달 경로가 관련되어 있는지를 확인할 수 있습니다. 이 과정에서 inhibitor나 siRNA를 사용하면 해당 반응에 관여하는 인자가 무엇인지 추가적으로 검증할 수 있습니다.
Firefly luciferase 기반의 pGL4 Vector는 다양한 response element와 조절 서열을 제공하여 신호전달 경로를 특성화하고 조절하는 데 활용할 수 있습니다. 예를 들어, CREB, CRE, STAT5RE 등이 포함한 벡터가 연구용으로 제공되며, 전체 목록은 Table 1에서 확인할 수 있습니다. 이러한 벡터 중 다수는 안정적으로 형질전환된 세포주 선별을 가능하게 하는 hygromycin 저항성 유전자를 포함하고 있습니다.
핵 수용체(Nuclear Receptor) 연구
생물발광 reporter gene은 핵 수용체(nuclear receptor)의 특성을 규명하는 데에도 활용될 수 있습니다. 핵 수용체는 세포 내에서 스테로이드나 기타 분자를 감지하는 리간드 의존적 전사 인자(ligand-regulated transcription factor)의 한 종류입니다. 일반적으로 핵 수용체는 세포질에 존재하며, 종종 관련 조절 단백질과 복합체를 형성하고 있습니다. 리간드가 결합하면, 수용체는 핵으로 이동(translocation) 하여 DNA 결합 도메인을 통해 특정 response elemen에 결합하고, 인접한 유전자의 발현을 증가시킵니다. 발광 reporter는 universal receptor assay로 핵 수용체의 작용제(agonist), 길항제(antagonist), co-repressor, co-activator를 규명하고 특성화하는 데 활용될 수 있습니다. 이 Universal nuclear receptor assay는 “one-hybrid assay”로 이해할 수 있는데, 여기서는 핵 수용체의 리간드 결합 도메인(LBD)을 yeast GAL4 전사인자와 융합되어 있으며, 리간드가 핵 수용체에 결합하면 firefly luciferase가 발현되게 됩니다(Figure 8).

Figure 8. Universal nuclear receptor assay
핵 수용체의 리간드 결합 도메인(ligand-binding domain)은 GAL4에 융합되어 있습니다. 세포 내에서 해당 리간드가 핵 수용체–GAL4 융합 단백질에 결합하면, 리간드 결합 도메인에 결합해 있던 co-repressor가 떨어져 나갑니다. 이어 co-activator가 transcription machinery를 luciferase reporter gene으로 유도하여 luciferase 발현이 일어나고, 결과적으로 발광(luminescence)이 증가합니다.
Universal nuclear receptor assay를 진행하기 위해서는, 먼저 관심 있는 세포주에 LBD-GAL4 DBD 융합 단백질을 발현하는 벡터와, 적절한 reporter 벡터(예: pGL4.35[luc2P/9XGAL4UAS/Hygro] Vector, Cat.# E1370)를 함께 co-transfection해야 합니다. 이 벡터에는 firefly luciferase reporter gene 발현을 유도하는 minimal promoter upstream에 GAL4 upstream activation sequence(UAS)가 여러 개 삽입되어 있어 reporter로 적합합니다. Transfection 2~3일 후, 관심 있는 테스트 화합물을 세포에 처리한 후 luciferase 활성을 측정합니다. 이 접근법을 통해 다양한 세포주를 핵 수용체 반응성 세포주로 전환할 수 있으며, 이를 통해 수용체 agonist, antagonist, co-activator, co-repressor를 규명할 수 있습니다. 또한, 리간드 결합 도메인에 돌연변이(mutagenesis)를 도입해 내인성 수용체의 간섭 없이 해당 반응성 세포주에서 그 효과를 평가할 수도 있습니다.
Universal nuclear receptor assay를 간소화하기 위해 사용할 수 있는 추가 시약들도 제공합니다. pBIND-Erα Vector (Cat.# E1390)는 yeast Gal4 DBD와 에스트로겐 수용체의 리간드 결합 도메인(ER-LBD)을 융합한 유전자를 포함합니다. pBIND-GR Vector (Cat.# E1581)는 yeast Gal4 DBD와 글루코코르티코이드 수용체의 리간드 결합 도메인(GR-LBD)을 융합한 유전자를 포함합니다. 또한, Promega는 pFN26A (BIND) hRluc-neo Flexi® Vector (Cat.# E1380)를 제공하며, 이 벡터는 GAL4 DBD, 링커 서열(linker segment), 그리고 프레임이 맞는 단백질 코딩 서열로 구성된 융합 단백질을 CMV early promoter의 조절하에 발현하도록 설계되었습니다. 각 BIND 벡터에는 Renilla luciferase/Neomycin 내성 유전자가 co-reporter로 포함되어 있어, transfection 효율을 보정하거나 추가적인 클로닝 과정 없이 double-stable cell line을 구축할 수 있습니다.
GPCR 연구
광범위한 생물학적 기능을 조절하며 신약 개발에서 가장 중요한 타겟 클래스 중 하나인 G protein-coupled receptor (GPCR)는 reporter gene을 이용해 연구할 수 있습니다 (Klabunde et al., 2002). Firefly luciferase 기반의 GloSensor™ GloSensor™ cAMP Assay는 세포 내 cAMP 농도의 변화를 통해 신호를 전달하는 과발현(overexpressed) 또는 내인성(endogenous) GPCR을 연구하는 데 민감하고 사용이 간편한 포맷을 제공합니다. 이 assay는 cAMP-binding domain과 Photinus pyralis luciferase의 mutant form을 융합한 genetically encoded biosensor variant를 사용합니다. cAMP가 결합하면 구조적 변화(conformational change)가 유도되어 발광 생성이 크게 증가시킵니다. Biosensor variant를 transient 또는 stable로 발현하는 세포에 GloSensor cAMP Reagent로 pre-equilibration 한 후, 이 biosensor를 이용하여 GPCR 기능을 분석하고, 살아 있는 세포에서 cAMP 축적이나 분해(turnover)를 동역학적으로 측정할 수 있습니다. 이 assay는 최대 500배에 달하는 발광 신호 변화를 제공하는 넓은 dynamic range를 가지며, forskolin과 같은 화합물로 인위적인 자극을 하지 않아도 Gi-coupled receptor activation이나 inverse agonist 활성까지 검출할 수 있습니다. 자세한 내용은 GloSensor™ Technology 페이지에서 확인할 수 있습니다.
GPCR Reporter Assay에 대한 추가 자료
Reporter cell line을 이용한 반응 경로 연구
GloResponse™ Cell Line은 최적화된 luciferase reporter 기술이 세포주에 통합된 형태로, native reporter 효소와 비교해 더 짧은 유도 시간과 높은 민감도를 제공하는 destabilized luc2P gene을 사용합니다. 예를 들어, GloResponse™ NFAT-RE-luc2P HEK293 Cell Line, NFκB-RE-luc2P HEK293 Cell Line, CRE-luc2P HEK293 Cell Line은 각각 NFAT, NF-κB, cAMP response pathway를 통해 reporter gene을 활성화시켜 세포 신호전달을 빠르고 편리하게 분석할 수 있습니다. 이들 세포주는 transfection을 통해 적절한 단백질을 도입하면 GPCR을 포함한 비내재성(non-native) activator도 연구할 수 있습니다. 이 세포주들은 clonal selection으로 제작되었으며, 관심 있는 pathway가 활성화되면 매우 높은 수준의 reporter induction을 보여줍니다.
GPCR 신호전달 경로는 관여하는 G protein α-subunit에 따라 Gs, Gi/o, Gq 세 가지 클래스로 나눌 수 있습니다. Gs- 및 Gi/o-coupled GPCR은 cAMP와 cAMP response element (CRE)를 통해 신호를 전달하므로, 이 경우 GloResponse™ CRE-luc2P HEK293 Cell Line을 사용할 수 있습니다. Gq-coupled GPCR은 칼슘 이온과 NFAT-RE를 통해 신호를 전달하므로, 이 경우에는 GloResponse™ NFAT-RE-luc2P HEK293 Cell Line을 사용합니다. GloResponse™ Cell Line을 활용한 GPCR assay는 high-throughput 스크리닝에 적합하며, 일반적인 assay 포맷보다 더 넓은 반응 범위(fold induction)를 가지며, 높은 Z′ 값으로 확인되듯 고품질 데이터를 제공합니다.
Protein Dynamics 연구
많은 신호전달 단백질의 turnover 속도는 엄격하게 조절됩니다. 세포 신호전달 이벤트나 세포 환경의 변화에 따라 단백질 안정화 및 축적이 일어나고, 이는 이후 하위 전사 이벤트의 활성화를 유도할 수 있습니다. NanoLuc® Stability Sensor Vectors (Cat.# N1381, N1391)는 HIF1A와 NRF2라는 두 가지 주요 신호 단백질의 안정성을 연구할 수 있도록 디자인되었으며, 각각 저산소(hypoxia)와 산화 스트레스(oxidative stress)가 세포에 미치는 영향을 직접적으로 측정할 수 있는 방법을 제공합니다(Robers et al., 2014). 이 벡터들은 NanoLuc® luciferase를 각 단백질의 C-말단에 융합하여, CMV promoter의 조절 하에서 발현되도록 구성되어 있습니다. Constitutive promoter인 CMV를 사용하기 때문에 발광 신호의 변화가 단백질 수준의 동적 변화를 직접적으로 반영합니다.
Protein Dynamics 연구에 대한 추가 자료
- Article: NanoLuc® Luciferase와 GloMax® Discover System을 이용한 생리학적 수준에서의 HIF1α 발현 검출
- Article: NanoLuc® Luciferase를 이용한 세포 내 Protein Lifetime Dynamics 측정
Protein Interaction 연구
단백질 간 상호작용(protein:protein interaction, PPI)을 모니터링하는 방법 중 하나는 bioluminescence resonance energy transfer(BRET)입니다. 이 때 두 가지 fusion protein을 만듭니다. 하나는 NanoLuc® 또는 Renilla luciferase 와 융합하고, 다른 하나는 형광 분자(fluorescent molecule)에 융합합니다. 두 단백질이 상호작용하면, 발광 분자로부터 형광 분자로 에너지가 전달되며, 빛이 blue에서 green으로 변화합니다(Angers et al., 2000). NanoLuc® luciferase를 energy donor로, HaloTag® protein에 결합된 NanoBRET® 618 fluorophore를 energy acceptor로 사용하는 경우, 기존 BRET assay보다 향상된 NanoBRET® PPI Assay를 구현할 수 있습니다. NanoLuc® donor에서 나오는 밝고 blue-shifted 신호와 HaloTag® acceptor의 far-red-shifted 신호가 결합하여, 기존 BRET assay보다 스펙트럼 중첩이 최적화되고, 신호는 강해지며, background는 낮은 protein interaction assay를 제공합니다.
또다른 단백질 상호작용 검출 방법은 structural complementation reporter system입니다. 관심 있는 단백질 각각에 리포터 단편(subunit)을 융합하여 세포에서 발현시키면, 두 단백질이 상호작용할 때 두 subunit이 결합하여 활성 효소(active enzyme)를 형성하고, 기질이 존재할 때 밝은 발광 신호를 생성합니다. NanoLuc® Binary Technology (NanoBiT)는 Large BiT(LgBiT)과 Small BiT(SmBiT)으로 구성되어 있으며, 이들이 결합해 NanoBiT® 효소가 형성됩니다. 이를 통해 실시간으로 단백질 상호작용 다이내믹스를 추적할 수 있습니다.
단백질 상호작용 연구에 대한 추가 자료
- 단백질:단백질 상호작용
- Article: BRET과 NanoLuc® Luciferase를 이용한 단백질 상호작용 연구
- Poster: NanoLuc® Binary Technology (NanoBiT)를 이용한 세포 내 단백질 상호작용 모니터링
세포 및 동물 이미징
Luciferase reporter gene은 세포 및 동물 모델에서 발광 리포터(light-emitting reporter)로 사용될 수 있습니다. Live-cell luciferase substrate나 분비형 luciferase를 사용하면 세포를 손상시키지 않고(non-destructive) 정량 분석을 수행할 수 있으며, 동일한 샘플에 대해 여러 번 측정이 가능합니다. NanoLuc® luciferase는 발광 이미징(bioluminescence imaging)에 매우 적합합니다. 작은 크기로 인해 NanoLuc®은 융합 파트너의 정상 기능에 미치는 영향이 적으며, 높은 발광 강도로 인해 단 몇 초의 노출 시간만으로 세포 내 소기관 수준의 위치(localization)를 모니터링할 수 있습니다. 자세한 내용은 imaging 관련 자료에서 확인할 수 있습니다.
Related Products and Resources
Categories
References
- Angers, S. et al. (2000) Detection of β2-adrenergic receptor dimerization in living cells using bioluminescence resonance energy transfer (BRET). Proc. Natl. Acad. Sci. USA 97, 3684–9.
- Brasier, A.R. and Ron, D. (1992) Luciferase reporter gene assay in mammalian cells. Methods Enzymol. 216, 386–97.
- Farfan, A. et al. (2004) Multiplexing homogeneous cell-based assays Cell Notes 10, 15–8.
- Faridi, J. et al. (2003) Expression of constitutively active Akt-3 in MCF-7 breast cancer cells reverses the estrogen and tamoxifen responsivity of these cells in vivo. Clin. Can. Res. 9, 2933–9.
- Hall, M.P. et al. (2012) Engineered luciferase reporter from a deep sea shrimp utilizing a novel imidazopyrazinone substrate. ACS Chem. Biol. 7, 1848–57.
- Hannah, R. et al. (1998) Rapid luciferase reporter assay systems for high-throughput studies. Promega Notes 65, 9–14.
- Hawkins, E.H. et al. (2002) Dual-Glo™ Luciferase Assay System: Convenient dual-reporter measurements in 96- and 384-well plates. Promega Notes 81, 22–6.
- Hirose, F. et al. (2002) Drosophila Mi-2 negatively regulates dDREF by inhibiting its DNA-binding activity. Mol. Cell. Biol. 22, 5182–93.
- Klabunde, T. and Hessler G. (2002) Drug design strategies for targeting G-protein-coupled receptors. Chembiochem. 4, 928–44.
- Klingenhoff, A. et al. (1999) Functional promoter modules can be detected by formal models independent of overall nucleotide sequence similarity. Bioinformatics 15, 180–6.
- Li, X. et al. (1998) Generation of destabilized green fluorescent protein as a transcription reporter. J. Biol. Chem. 273, 34970–5.
- Robers, M. et al. (2014) Measuring intracellular protein lifetime dynamics using NanoLuc® luciferase. PubHub.
- Wood, K.V. (1998) The chemistry of bioluminescent reporter assays. Promega Notes 65, 14–20.
- Zakowicz, H. et al. (2008) Measuring cell health and viability sequentially by same-well multiplexing using the GloMax ® -Multi Detection System. Promega Notes 99, 25–8.
- Zhuang, F. and Liu, Y.H. (2006) Usefulness of the luciferase reporter system to test the efficacy of siRNA. Methods Mol. Biol. 342, 181–7.
Appendix: Vector and Reporter Assay Listings
| Table 1. pGL4 Luciferase Reporter Vectors. | |||||
| Vector | Reporter Gene | Multiple Cloning Region | Protein Degradation Sequence | Gene Promoter | Mammalian Selectable Marker |
|---|---|---|---|---|---|
| pGL4.10 | luc2 | Yes | No | No | No |
| pGL4.11 | luc2P | Yes | hPEST | No | No |
| pGL4.12 | luc2CP | Yes | CL1-hPEST | No | No |
| pGL4.13 | luc2 | No | No | SV40 | No |
| pGL4.14 | luc2 | Yes | No | No | Hygro |
| pGL4.15 | luc2P | Yes | hPEST | No | Hygro |
| pGL4.16 | luc2CP | Yes | CL1-hPEST | No | Hygro |
| pGL4.17 | luc2 | Yes | No | No | Neo |
| pGL4.18 | luc2P | Yes | hPEST | No | Neo |
| pGL4.19 | luc2CP | Yes | CL1-hPEST | No | Neo |
| pGL4.20 | luc2 | Yes | No | No | Puro |
| pGL4.21 | luc2P | Yes | hPEST | No | Puro |
| pGL4.22 | luc2CP | Yes | CL1-hPEST | No | Puro |
| pGL4.23 | luc2 | Yes | No | minP | No |
| pGL4.24 | luc2P | Yes | hPEST | minP | No |
| pGL4.25 | luc2CP | Yes | CL1-hPEST | minP | No |
| pGL4.26 | luc2 | Yes | No | minP | Hygro |
| pGL4.27 | luc2P | Yes | hPEST | minP | Hygro |
| pGL4.28 | luc2CP | Yes | CL1-hPEST | minP | Hygro |
| pGL4.29 | luc2P | No | hPEST | minP + CRE | Hygro |
| pGL4.30 | luc2P | No | hPEST | minP + NFAT RE | Hygro |
| pGL4.31 | luc2P | No | hPEST | adenovirus major late + GAL4 UAS | Hygro |
| pGL4.32 | luc2P | No | hPEST | minP + NF-kB RE | Hygro |
| pGL4.33 | luc2P | No | hPEST | serum response element | Hygro |
| pGL4.34 | luc2P | No | hPEST | SRF RE | Hygro |
| pGL4.35 | luc2P | No | hPEST | GAL4 UAS | Hygro |
| pGL4.36 | luc2P | No | hPEST | murine mammary tumor virus long terminal repeat | Hygro |
| pGL4.37 | luc2P | No | hPEST | minP + antioxidant RE | Hygro |
| pGL4.38 | luc2P | No | hPEST | minP + p53 RE | Hygro |
| pGL4.39 | luc2P | No | hPEST | minP + ATF6 RE | Hygro |
| pGL4.40 | luc2P | No | hPEST | minP + metal RE | Hygro |
| pGL4.41 | luc2P | No | hPEST | minP + heat shock RE | Hygro |
| pGL4.42 | luc2P | No | hPEST | minP + hypoxia RE | Hygro |
| pGL4.43 | luc2P | No | hPEST | minP + xenobiotic RE | Hygro |
| pGL4.44 | luc2P | No | hPEST | minP + AP1 RE | Hygro |
| pGL4.45 | luc2P | No | hPEST | minP + interferon stimulated RE | Hygro |
| pGL4.47 | luc2P | No | hPEST | minP + Sis-inducible element RE | Hygro |
| pGL4.48 | luc2P | No | hPEST | minP + SMAD3/SMAD4 binding element RE | Hygro |
| pGL4.49 | luc2P | No | hPEST | minP + TCF-LEF RE | Hygro |
| pGL4.50 | luc2 | No | No | CMV | Hygro |
| pGL4.51 | luc2 | No | No | CMV | Neo |
| pGL4.52 | luc2P | No | hPEST | minP + STAT5 RE | Hygro |
| pGL4.53 | luc2 | No | No | phosphoglycerate kinase (PGK) | No |
| pGL4.54 | luc2 | No | No | thymidine kinase (TK) | No |
| pGL4.70 | hRluc | Yes | No | No | No |
| pGL4.71 | hRlucP | Yes | hPEST | No | No |
| pGL4.72 | hRlucCP | Yes | CL1-hPEST | No | No |
| pGL4.73 | hRluc | No | No | SV40 | No |
| pGL4.74 | hRluc | No | No | HSV-TK | No |
| pGL4.75 | hRluc | No | No | CMV | No |
| pGL4.76 | hRluc | Yes | No | No | Hygro |
| pGL4.77 | hRlucP | Yes | hPEST | No | Hygro |
| pGL4.78 | hRlucCP | Yes | No | No | Hygro |
| pGL4.79 | hRluc | Yes | No | No | Neo |
| pGL4.80 | hRlucP | Yes | hPEST | No | Neo |
| pGL4.81 | hRlucCP | Yes | CL1-hPEST | No | Neo |
| pGL4.82 | hRluc | Yes | No | No | Puro |
| pGL4.83 | hRlucP | Yes | hPEST | No | Puro |
| pGL4.84 | hRlucCP | Yes | CL1-hPEST | No | Puro |
| Table 2. pNL Reporter Vectors. | |||||
| Vector | Reporter Gene | Multiple Cloning Region | Protein Degradation Sequence | Gene Promoter | Mammalian Selectable Marker |
|---|---|---|---|---|---|
| pNL1.1[Nluc] | Nluc | Yes | No | No | No |
| pNL1.1.CMV[Nluc/CMV] | Nluc | No | No | CMV | No |
| pNL1.2[NlucP] | NlucP | Yes | hPEST | No | No |
| pNL1.3[secNluc] | secNluc | Yes | No | No | No |
| pNL1.3.CMV [secNluc/CMV] | secNluc | No | No | CMV | No |
| pNL2.1[Nluc/Hygro] | Nluc | Yes | No | No | Hygro |
| pNL2.2[NlucP/Hygro] | NlucP | Yes | hPEST | No | Hygro |
| pNL2.3[secNluc/Hygro] | secNluc | Yes | No | No | Hygro |
| pNL3.1[Nluc/minP] | Nluc | Yes | No | minP | No |
| pNL3.2.CMV | NlucP | No | hPEST | CMV | No |
| pNL3.2.NF-κB-RE [NlucP/NF-κB-RE/ Hygro] | NlucP | No | hPEST | minP | Hygro |
| pNL3.2[NlucP/minP] | NlucP | Yes | hPEST | minP | No |
| pNL3.3[secNluc/minP] | secNluc | Yes | No | minP | No |
| pNLCoI1[luc2-P2A-NlucP/Hyg] | luc2, NlucP | Yes | Yes for NlucP, No for luc2 |
No | Hygro |
| pNLCoI2[luc2-P2A-Nluc/minP/Hyg] | luc2, NlucP | Yes | Yes for NlucP, No for luc2 |
minP | Hygro |
| pNLCoI3[luc2-P2A-NlucP/CMV/Hyg] | luc2, NlucP | No | Yes for NlucP, No for luc2 |
CMV | Hygro |
| pNLCoI4[luc2-P2A-NlucP/PGK/Hyg] | luc2, NlucP | No | Yes for NlucP, No for luc2 |
PGK | Hygro |
| Table 3. Luciferase Reporter Assays. | ||||
| Assay System | Gene Assayed | Single-Sample or Plate Assay | Signal Stability | Live-Cell Assay |
|---|---|---|---|---|
| Single Reporter | ||||
| Nano-Glo® Luciferase Assay System | Nluc, secNluc | Single or Plate2 | Long (≥2.0h) | Yes3 |
| Luciferase Assay System | luc, luc+, luc2 | Single or Plate1 | Short (<0.5h) | No |
| Steady-Glo® Luciferase Assay System | luc, luc+, luc2 | Plate2 | Long (>0.5h) | No |
| Bright-Glo™ Luciferase Assay System | luc, luc+, luc2 | Plate2 | Long (>0.5h) | No |
| ONE-Glo™ Luciferase Assay System | luc, luc+, luc2 | Plate2 | Long (≥45 minutes) | No |
| ONE-Glo™ EX Luciferase Assay System | luc, luc+, luc2 | Plate2 | Long (≥2 hours) | No |
| Renilla Luciferase Assay System | Rluc, hRluc | Single or Plate1 | Short (<0.5h) | No |
| Renilla-Glo® Luciferase Assay System | Rluc, hRluc | Plate2 | Long (≥60 minutes) | No |
| Dual Reporter | ||||
| Nano-Glo® Dual-Luciferase® Reporter Assay System | Nluc, luc, luc+, luc2 | Plate2 | Long (≥2h) | No |
| Dual-Glo® Luciferase Assay System | luc+, luc2, Rluc, hRluc | Plate2 | Long (>0.5h) | No |
| Dual-Luciferase® Reporter Assay System | luc+, luc2, Rluc, hRluc | Single (Cat.# E1910) | Short (<0.5h) | No |
|
|
|
Plate1 (Cat.# E1980) | Short (<0.5h) | No |
| Live-Cell | ||||
| Nano-Glo® Live Cell Assay System | Nluc | Plate | Short | Yes |
| Nano-Glo® Vivazine™ Live Cell Substrate | Nluc | Plate | Long | Yes |
| Nano-Glo® Endurazine™ Live Cell Substrate | Nluc | Plate | Long | Yes |
| EnduRen™ Live Cell Substrate | Rluc, hRluc | Plate1 | Long (>0.5h) | Yes |
| ViviRen™ Live Cell Substrate | Rluc, hRluc | Plate | Short (<0.5h) | Yes |
1Use with plates only when the luminometer has a reagent injector.
2We do not recommend the use of this product with automated reagent injectors.
3Use for live-cell assays by quantifying the secreted form of NanoLuc® luciferase in culture medium.