Cell Viability 및 Cytotoxicity Assay 선택 가이드
본 가이드는 cell viability와 cytotoxicity assay의 원리를 설명하고, 연구 목적에 적합한 cell health assay를 선택하는 도움이 되는 정보를 제공합니다. 본문에서 언급된 분석법의 주문 정보는 Cell Viability and Cytotoxicity Assays 제품 목록에서 확인 가능합니다.
Johanna Lee and Mariel Mohns
Promega Corporation
Publication Date: 06/2019; tpub_209
다양한 Cell Viability(세포 생존율) 및 Cytotoxicity(세포 독성) assay중에서 적합한 방법을 선택하는 일은 생각보다 쉽지 않을 수 있습니다. 연구 목적에 부합하는 최적의 cell health assay를 선택하려면, 각 분석법이 어떤 지표(marker)를 측정하는지, 그 측정값이 세포 생존율과 어떤 연관성이 있는지, 그리고 각 분석 화학 반응(assay chemistry)의 한계점은 무엇인지에 대한 이해가 필요합니다. 또한, 호환 가능한 분석법을 동시에 사용하면(multiplexing), 하나의 샘플로부터 더 많은 데이터를 얻을 수 있으며, 통계적 신뢰도 또한 높일 수 있습니다.
본 가이드에서는 plate reader 기반 검출 방법과 간편한 “add–mix–measure” 프로토콜을 사용하는 Promega의 cell viability 및 cytotoxicity assay를 소개합니다. 또한, cell health assay를 선택할 때 고려해야 할 핵심 요소를 함께 제시하여, well 간(well-to-well), plate간(plate-to-plate), 그리고 일자 간(day-to-day) 데이터도 민감하게 비교 해석할 수 있도록 지원합니다.
세포 기반 분석법을 통해 배양 세포에서 살아있는 세포(live cell), 죽은 세포(dead cell) 그리고 세포사멸(apoptosis), 자가포식(autophagy), 산화 스트레스(oxidative stress) 상태에 있는 세포를 측정하는 방법을 확인해 보세요.

Cell Viability Assay 소개
Cell viability assay는 대사 활성이 있는(살아있는) 세포를 나타내는 다양한 지표를 이용합니다. 일반적으로 사용되는 지표로는 ATP 농도, 기질 환원 능력, 그리고 살아있는 세포에만 존재하는 효소 및 protease 활성 등이 있습니다.
Real-time Cell Viability Assays
RealTime-Glo™ MT Cell Viability Assay(Cat.# G9711)는 세포 생존율을 실시간으로 측정하는 분석법입니다. 이 assay에서는 엔지니어링 된 luciferase와 pro-substrate(luciferase의 기질이 아님)를 세포 배양 배지에 직접 첨가합니다. 이 pro-substrate는 세포막을 통과하여 세포 내부로 들어가며, 대사 활성이 있는 살아있는 세포에서만 pro-substrate가 luciferase 반응에 사용 가능한 기질(substrate)로 환원됩니다(Figure 1). 이 환원된 기질은 세포 밖으로 확산되어 검출 시약(detection reagent) 내 luciferase에 의해 발광 신호를 생성합니다. 이 방법은 최대 3일 동안 동일한 well에서 반복 측정이 가능합니다. 이 분석법의 주요 장점은 적은 수의 plate와 세포만으로도 dose–response 관계를 실시간으로 모니터링할 수 있으며, 세포를 용해하지 않기 때문에 추가적인 세포 기반 분석(cell-based assay) 또는 후속 응용 실험에도 동일 세포를 활용할 수 있다는 점입니다.
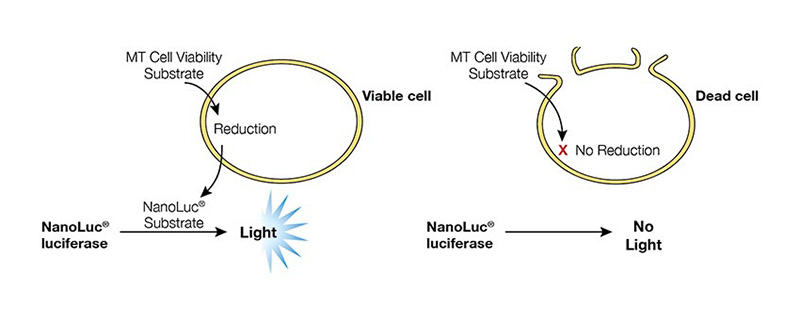
Figure 1. RealTime-Glo™ MT Cell Viability Assay 원리
ATP Cell Viability Assays
ATP는 살아있는 세포만이 합성할 수 있는 분자이기 때문에, 세포 생존율의 측정 지표로 활용할 수 있습니다.CellTiter-Glo® Luminescent Cell Viability Assay(Cat.# G7570)는 detergent, 안정화된 luciferase, 그리고luciferin 기질이 포함된 시약을 사용하여 ATP를 정량 합니다. Detergent는 생존 세포를 용해시켜 세포 내 ATP를 배지로 방출시키며, ATP 존재 하에 luciferase가 luciferin을 이용해 발광 신호를 생성합니다. 이 신호는 luminometer를 사용해 10분 이내로 쉽게 측정할 수 있습니다 (Figure 2). CellTiter-Glo® 2.0 Assay(Cat.# G9241)는 간편하게 사용할 수 있도록 단일 용액 형태로 제공되어 시약 준비 시간을 줄이고, 상온 보관이 가능하도록 설계되었습니다. 이러한 ATP 기반 분석법은 기질을 색상 변화(검출 가능한 형태)로 전환하기 위해 긴 incubation 시간이 필요한 다른 방법보다 훨씬 빠르며, 높은 감도(sensitivity)와 넓은 선형성(linearity)을 제공하므로 소량의 세포를 사용하는 high-throughput 실험에도 매우 적합합니다. 또한, 다른 분석법에 비해 비특이적 신호(artifacts)가 적어 데이터의 신뢰성이 높습니다.

Figure 2. CellTiter-Glo® Assay는 생존 세포의 지표로 ATP를 측정합니다.
Live-Cell Protease Viability Assay
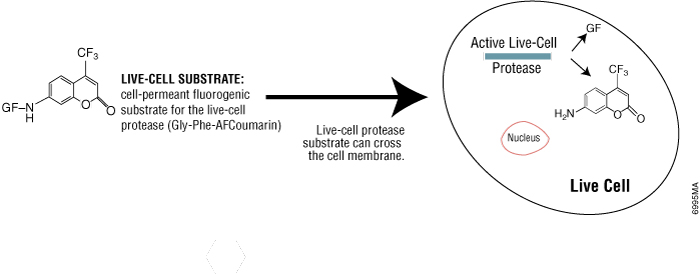
살아있는 세포에서만 활성이 유지되는 protease(Live-cell protease)는 세포 사멸 시 빠르게 소실되기 때문에, 생존 세포를 구별하는 유용한 지표로 사용됩니다. CellTiter-Fluor™ Cell Viability Assay (Cat.# G6080)는 세포 투과성을 가진 형광 기반 protease 기질인 GF-AFC(fluorogenic protease substrate)를 통해 살아있는 세포 내 protease 활성을 직접 측정합니다. 이 기질은 살아있는 세포 안으로 들어가며 protease에 의해 절단되어, 살아있는 세포 수에 비례하는 형광 신호를 생성합니다(Figure 3). 이 방법의 incubation 시간은 0.5–1시간으로, tetrazolium 기반 분석법(1–4시간)에 비해 훨씬 짧으며, 세포 용해가 필요하지 않기 때문에, 동일한 샘플 well에서 세포 기반 발광 리포터 분석(bioluminescent reporter assay)과 같은 다른 분석법과 multiplexing이 가능합니다.
Tetrazolium Reduction Cell Viability Assays
생존 세포 검출에 사용되는 tetrazolium 화합물은 크게 두 가지 형태로 분류할 수 있습니다:
1. 세포 투과성의 양전하 화합물 (MTT)
대사 활성이 있는 생존 세포는 MTT를 보라색을 띠는 formazan으로 환원할 수 있습니다. 따라서 색의 발생은 생존 세포의 유용한 지표로 활용할 수 있습니다. CellTiter 96® Non-Radioactive Cell Proliferation Assay (MTT) (Cat.# G4000)는 이러한 원리를 이용한 대표적인 분석법입니다. 다만, 이 방법은 긴 incubation 시간(약 4시간)이 필요하며, 생성된 formazan이 불용성(insoluble)이기 때문에 흡광도 측정 전에 용해 시약을 추가해야 합니다.
세포 불투과성의 음전하 화합물 (MTS, XTT, WST-1)
CellTiter 96® AQueous One Solution Cell Proliferation Assay (MTS) (Cat.# G3582)는 음전하를 띤 tetrazolium 화합물을 사용합니다. 음전하 화합물은 세포 내부로 들어가지 못하므로 전자 전달 매개체(intermediate electron coupling reagent)를 함께 사용해야 하며, 이 전자 전달 매개체는 세포 안으로 들어가 환원된 후 다시 세포 밖으로 나와 tetrazolium을 수용성의 formazan으로 변환시킵니다. Incubation 시간은 약 1–4시간이며, formazan 생성물이 수용성이기 때문에 별도의 용해 과정이 필요하지 않아 보다 간편하게 사용할 수 있습니다.
Resazurin Reduction Cell Viability Assay
Resazurin은 세포 투과성이 있는 지시 염료(indicator dye)로, 짙은 파란색을 띠며 자체 형광이 거의 없습니다. CellTiter-Blue® Cell Viability Assay(Cat.# G8080)는 이 resazurin을 이용해 세포 생존율을 측정합니다. 대사 활성이 있는 살아있는 세포만이 resazurin을 형광 신호를 내는 분홍색 resorufin으로 환원시킬 수 있습니다. 약 1–4시간의 incubation 후, 생성된 신호는 microplate spectrophotometer 또는 fluorometer를 이용해 정량 할 수 있습니다. 이 방법은 비교적 비용이 저렴하면서도 tetrazolium 기반 분석보다 높은 감도를 제공합니다. 단, 실험에 사용되는 일부 화합물이 resorufin 형광 신호와 간섭할 수 있다는 점은 주의해야 합니다.
Tetrazolium 또는 resazurin 환원 기반 분석법의 공통적인 한계점은 측정 시간이 지남에 따라 축적되는 색 변화 또는 형광 생성물의 누적에 의존한다는 점입니다. 따라서 이러한 신호가 시간이 지남에 따라 점진적으로 증가하기 때문에, 긴 incubation 시간 동안 세포 생존율이 감소하는 것을 즉각적으로 감지할 수 없습니다.
Cytotoxicity Assay 소개
세포 사멸(cell death) 후 일어나는 주요 변화 중 하나는 세포막 무결성(membrane integrity)의 상실입니다. 이로 인해 세포 내부에 존재하던 단백질이나 화합물이 외부로 유출되거나, 외부 물질이 세포 안으로 쉽게 침투하게 됩니다. 여기서는 세포 사멸 시 방출되는 단백질(dead-cell protease, lactate dehydrogenase)이나 세포 내로 유입되는 화학물질(DNA dye)을 검출하여 사멸 세포의 존재를 평가하는 cytotoxicity assay를 소개합니다.
Dead-cell Protease Release Cytotoxicity Assay
세포가 죽어 세포막이 손상되면, dead-cell protease가 세포 밖으로 방출됩니다. 이때, 발광성 기질을 사용하는 CytoTox-Glo™ Cytotoxicity Assay(Cat.# G9290)나 형광성 기질을 사용하는 CytoTox-Fluor™ Cytotoxicity Assay(Cat.# G9260)를 통해 dead-cell protease 활성을 측정할 수 있습니다(Figure 4). 이 두 기질은 세포를 투과하지 못하므로, 세포막이 온전한 살아있는 세포에서는 신호가 거의 발생하지 않습니다. 또한, 이는 세포를 용해하지 않는non-lytic 방식이므로, 다른 분석법과 multiplexing하여 동일한 샘플에서 추가적인 세포 기반 분석을 수행할 수도 있습니다.
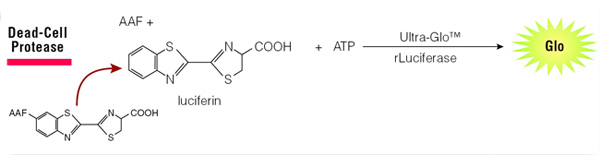
Figure 4. CytoTox-Glo® Assay는 세포 사멸에 따라 방출되는 protease를 측정합니다.
Lactate Dehydrogenase (LDH) Release Cytotoxicity Assays
세포막 무결성을 잃은 사멸 세포는 LDH(Lactate Dehydrogenase)를 세포 밖으로 방출합니다. LDH는 젖산(lactate)을 피루브산(pyruvate)으로 전환시키는 반응을 촉매하며, 이 과정에서 NADH가 생성됩니다. 따라서 과량의 기질(lactate와 NAD⁺)을 제공하면 방출된 LDH의 활성을 생성된 NADH 양을 통해 측정할 수 있습니다. 이렇게 생성된 NADH는 서로 다른 분석 화학법을 통해 정량할 수 있습니다.
1. LDH-Glo™ Cytotoxicity Assay
LDH-Glo™ Cytotoxicity Assay (Cat.# J2380)에서는 환원효소(reductase)가 NADH와 환원효소 기질(proluciferin)을 이용해 luciferin을 생성합니다. 생성된 luciferin은 Promega의 독자적인 luciferase(Ultra-GloTM rLuciferase)에 의해 발광 반응을 일으키며, 발광 세기는 LDH의 양에 비례합니다. 생성된 신호는 luminometer를 통해 측정할 수 있습니다.

2. CytoTox-ONE™ Homogenous Membrane Integrity Assay
CytoTox-ONE™ Homogeneous Membrane Integrity Assay (Cat.# G7890)는 resazurin을 형광성 resorufin으로 전환시키는 반응을 기반으로 하며, 생성된 형광 신호는 fluorometer를 통해 측정합니다.

Figure 6. CytoTox-ONE™ Assay는 resazurin의 환원으로 생성된 형광성 resorufin을 측정합니다.
3. CytoTox 96® Non-Radioactive Cytotoxicity Assay
CytoTox 96® Non-Radioactive Cytotoxicity Assay(Cat.# G1780)는 tetrazolium salt(INT)가 붉은색을 띠는 formazan으로 전환되는 반응을 통해 검출하며, 생성된 색 변화는 흡광도로 측정합니다.

Figure 7. CytoTox-96® Assay는 tetrazolium salt(INT)가 붉은색의 formazan 생성물로 전환된 양을 측정합니다.
DNA Dye Cytotoxicity Assay
일부 DNA 결합 염색 시약(DNA-binding dye)은 살아있는 세포에는 침투하지 못하지만, 막이 손상된 죽은 세포 내부로 들어가 DNA를 염색할 수 있습니다. Trypan blue와 같은 전통적인 염색 시약은 보통 염색된 세포를 혈구계수기(hemocytometer)로 직접 세어야 하므로 수작업이 많이 필요하고 대량 분석에는 적합하지 않습니다. 또한, 이러한 전통적인 염색 시약은 세포 독성을 나타낼 수 있으며, 실시간 측정이 아닌 endpoint 분석에만 사용할 수 있다는 한계가 있습니다.
CellTox™ Green Dye와 같은 최신 염색 시약은 DNA에 결합할 때 형광 신호를 생성하며, 이 신호는 fluorometer를 이용해 손쉽게 정량화 할 수 있습니다. 이 염색 시약은 배양액에 희석하여 cell seeding 시 직접 첨가하거나 약물과 함께 첨가할 수 있으며, 이를 통해 실시간 kinetic 분석이 가능합니다. CellTox™ Green Cytotoxicity Assay (Cat.# G8741)는 세포 독성이 없고 높은 광안정성(photo-stability)을 가지며, 쉽게 확장 가능한 세포 독성 분석법입니다.
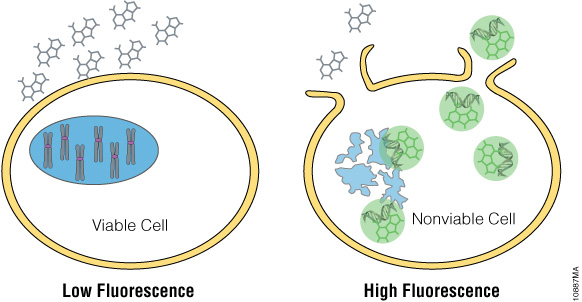
Figure 8. CellTox™ Green은 형광성 DNA 결합 염색 시약으로 세포 사멸 시 방출된 DNA를 검출합니다.
Cell Health Assay는 어떻게 선택할까요?
적절한 cell health assay를 선택하는 일은 쉽지 않습니다. 여기에서는 매뉴얼 방식이나 자동화된 분석 시스템에서 사용할 세포 기반 분석법(cell-based assay)을 선택할 때 고려해야 할 주요 요인들을 소개합니다.
무엇을 측정하고 싶은가요?
실험 종료 시점에서 측정하고자 하는 세포는 살아있는 세포(viable cell)인가요, 아니면 죽은 세포(dead cell)인가요? Cell health assay는 살아있는 세포의 수를 측정하는 viability assay, 죽은 세포의 수를 검출하는 cytotoxicity assay, 그리고 세포 사멸 기전을 평가하는 apoptosis assay가 있습니다. 만약 실험의 목적이 단순히 “대조군(no treatment)”과 “실험군(toxin treatment)” 간의 차이 유무를 확인하는 것이라면, 살아있는 세포 수를 측정하든 죽은 세포 수를 측정하든 큰 차이는 없습니다. 하지만 세포 사멸의 구체적인 기작(mechanism)을 규명하려는 경우에는 독성 물질의 노출 시간(duration of exposure), 농도(concentration), 그리고 측정 시점(assay endpoint)이 매우 중요합니다(1). 이러한 요인들을 종합적으로 고려하면 무엇을 측정하고 싶은지를 결정하고 어떤 분석법이 가장 적합한지를 판단하는 데 도움이 됩니다.
어떤 모델 시스템을 사용하고 있나요?
Cell health 연구에서 사용하는 세포 origin과 세포 유형(type)은 대부분 연구 목적이나 분석 대상 약물 타겟에 의해 결정됩니다. 모델 시스템이 무엇이든, 세포 배양 및 assay plate 세팅 과정에서 일관되고 재현성 있는 절차를 확립하는 것이 매우 중요합니다. Well 당 세포 수나 분석 전 equilibration 시간과 같은 변동 요소는 세포의 생리적 상태에 영향을 줄 수 있습니다. 세포주의 유지 관리는 각 단계에서 표준화되고 검증되어야 하며, 양성 대조군(positive control)과 음성 대조군(negative control)을 실험 전반에 걸쳐 사용하여 세포의 생리적 상태를 일관되게 파악해야 합니다. 또한, 세포 유형이나 2D 배양인지 3D 배양인지에 따라 샘플 특성이 달라질 수 있으므로, 각 배양 모델 시스템마다 분석 절차를 별도로 검증해야 합니다. 소량의 세포(예: primary cell이나 제한된 세포 유형)만 사용할 수 있는 모델 시스템의 경우, 더 높은 감도를 가진 분석법이 필요합니다.
2D 또는 3D 세포 배양을 사용하고 있나요?
배양 세포는 생체 내(in vivo) 환경을 모사한 모델 시스템일 뿐, 실제 생체 내 세포와는 다릅니다. 이러한 차이를 줄이기 위해 최근 많은 연구자들이 3D 세포 배양(3D cell culture)을 사용하여 생체 내 조건을 더 가깝게 모사하고 있습니다. 2D 배양에서는 세포를 plate 표면에 단층으로 키우는 반면, 3D 배양에서는 세포들이 서로 상호작용하며 세포 간 연결(cell:cell connection)을 형성하는 구조 안에서 성장합니다. 이러한 구조적 복잡성으로 인해 분석 시약이 크기가 큰 microtissue의 중심부까지 도달하기 어렵고, lytic assay가 3D 시스템 내부의 모든 세포를 충분히 파괴하지 못할 수 있기 때문에 세포 기반 분석 수행 시 새로운 실험 설계상의 도전 과제를 야기합니다. 따라서, 3D 시스템에서는 시약에 더 강한 detergent를 포함시키고 기계적 파괴(mechanical disruption)를 적용하고 incubation 시간을 늘리는 등의 방법으로 실험 조건을 3D에 맞추어 최적화하는 과정이 필요할 수 있습니다. 또한, MTT와 같은 발색 기반(colorimetric) 분석법은 여러 겹의 세포층을 충분히 침투하기 어려워 3D 배양에는 적절하지 않습니다.
CellTiter-Glo® 3D Cell Viability Assay(Cat.# G9681)는 3D 배양 모델에서 세포 생존율을 측정하도록 특별히 설계된 분석법입니다. 이 분석 시약은 향상된 용해 능력을 갖추고 있어 큰 spheroid 샘플 내부로 잘 침투하여 다른 분석법에 비해 더 정확한 생존율 측정이 가능합니다. 또한, CellTiter-Glo® 3D Assay 시약은 ATP를 생존 지표로 측정하고 발광 신호를 생성합니다. 이는 흡광 또는 형광 기반 방법보다 훨씬 높은 감도를 제공합니다.
화합물의 세포 독성을 3D 배양에서 평가할 때에는 LDH-Glo™ Cytotoxicity Assay (Cat.# J2380)가 적합합니다. 이 방법은 세포막 침투에 의존하지 않고, 죽은 세포에서 배지로 방출된 LDH를 직접 측정합니다. 소량의 배지(2–5µl)만을 사용하여 측정이 가능하므로, 시간 경과에 따른 반복 샘플링이 가능합니다. 이를 통해 microtissues를 보존하고 남아 있는 생존 세포를 유지할 수 있며, 동일한 샘플을 다른 세포 기반 분석법이나 핵산 분석 등 downstream application에 활용하여 같은 샘플로 더 많은 데이터를 확보할 수 있습니다.
Cell health assay는 언제 수행하는 것이 적합할까요?
적절한 cell health assay를 수행하기 위해서는, 측정하고자 하는 분석 지표(assay marker)를 얻고자 하는 정보와 일치하도록 선택하는 것이 매우 중요합니다. 세포 사멸의 각 기전에 따라 발생하는 변화를 이해하면 어떤 분석법을 사용해야 하는지 결정하는 데 큰 도움이 됩니다. Figure 9는 apoptosis와 necrosis 과정에서 시간에 따라 일어나는 변화를 단순화하여 보여주는 예시이며, 각 시점에서 서로 다른 지표를 측정하는 분석법을 사용했을 때 예상되는 결과가 어떻게 달라지는지를 나타냅니다.

Figure 9. 세포 사멸 기전은 cell viability, cytotoxicity 그리고 apoptosis의 서로 다른 지표를 측정함으로써 in vitro에서 구별할 수 있습니다.
Necrosis가 진행 중인 세포는 일반적으로 빠른 팽창(swelling)을 보이며, 세포막 무결성을 상실하고, 대사 활동이 중단되고 세포질 성분을 주변 배양액으로 방출합니다. In vitro에서 급격한 necrosis가 일어나는 세포는 apoptosis 기작을 활성화할 충분한 시간이나 에너지를 확보하지 못하기 때문에, apoptosis 관련 지표를 발현하지 않습니다.
배양 중인 세포가 in vitro에서 apoptosis를 겪을 경우, 시간이 지남에 따라 결국 secondary necrosis로 진행됩니다. 오랜 시간 동안 배양하면, apoptotic 세포는 결국 대사 활동을 멈추고, caspase를 활성화하며, phosphatidylserine(PS)을 세포막 바깥쪽으로 노출시키고, 세포막 무결성을 상실하면서 세포질 성분을 배양액으로 방출하게 됩니다. 이때 caspase 활성이나 세포 표면의 PS 노출과 같은 apoptosis 지표는 일시적으로만 나타날 수 있습니다. 따라서 세포 사멸의 주요 기전을 규명하기 위해서는, 사용 중인 모델 시스템에서 세포 사멸이 진행되는 시간적 변화(kinetics)를 이해하는 것이 매우 중요합니다. 중요한 시점을 놓치지 않기 위해, 하나의 well에서 시간 경과에 따라 반복 측정이 가능한 비용해성 실시간 분석법(nonlytic real-time assay)을 선택하는 것이 좋습니다. 예를 들어, RealTime-Glo™ Annexin V Apoptosis and Necrosis Assay(Cat.# JA1011)와 같은 제품을 사용하면, 세포를 파괴하지 않고 동일한 well에서 여러 시점의 데이터를 수집할 수 있습니다.
여러 시점에서 데이터를 수집해야 하나요?
Live-cell kinetic assays 는 하나의 샘플 well에서 여러 time point에 걸쳐 반복적으로 측정할 수 있는 검출 시약입니다. 이러한 방식은 실험에 소요되는 시간과 노력을 줄여줄 뿐 아니라, 실시간(real-time)으로 더 유용한 데이터를 얻을 수 있게 합니다. 약물의 독성 발현 시점이나 작용 기전을 규명하기 위해 시간 의존성(time-response) 및 농도 의존성(dose-response) 실험을 진행해야 하는 경우, 실시간 분석이 특히 유용합니다. 세포 수가 제한적이거나 소중한 샘플을 사용하는 경우에는, 하나의 샘플로부터 가능한 한 많은 데이터를 얻는 것이 무엇보다 중요합니다. Promega는 live-cell kinetic 방식의 cell health 분석을 지원하는다양한 assay 를 제공합니다.
The RealTime-Glo™ MT Cell Viability Assay (Cat.# G9711)는 동일한 샘플 well에서 최대 72시간까지 세포 생존율을 지속적으로 모니터링할 수 있습니다. 이 분석법은 살아있는 세포의 환원력을 측정하며, ATP 비의존적이기 때문에 생존율 측정의 보완적 방법으로 활용할 수 있습니다. 또한, RealTime-Glo™ Annexin V Apoptosis and Necrosis Assay (Cat.# JA1011)는 apoptosis 과정 중 세포막 외부에 노출되는 phosphatidylserine(PS)을 실시간으로 측정할 수 있는 plate reader 기반 분석법입니다. 이 분석은 발광 신호(luminescent, apoptotic)와 형광 신호(fluorescent, necrotic)의 조합과 타이밍을 통해 secondary necrosis와 다른 유형의 cytotoxicity로 인한 necrosis를 구분할 수 있습니다. CellTox™ Green Cytotoxicity Assay (Cat.# G8741)는 세포막이 손상된 세포의 DNA에 결합하여 형광 신호를 생성하는 염색 시약(dye)을 사용합니다. 이 제품은 세포를 seeding할 때나 화합물을 처리할 때 등 어떤 incubation 시점에서든 바로 적용 가능하며, 세포 독성의 발현 시점을 실시간으로 모니터링할 수 있습니다.
이러한 assay들은 세포 독성이 없고 비용해(non-lytic) 방식이기 때문에, 실험 후에도 살아 있는 세포는 그대로 유지됩니다. 따라서, 후속 실험에도 활용 가능하며 하나의 샘플로부터 더 많은 데이터를 얻을 수 있습니다.
얼마나 많은 샘플을 측정해야 하나요?
측정해야 할 샘플 수가 한 개 또는 수 개 정도라면, 혈구계수기(hemacytometer)를 이용해 살아있는 세포나 죽은 세포를 수동으로 계수하는 방법으로도 충분할 수 있습니다. 이미지 분석이나 유세포 분석(flow cytometry)도 소량 샘플 측정에 유용하지만, 이러한 방법들은 고처리량(high-throughput) 분석에는 적합하지 않습니다. 반면, 많은 수의 샘플을 측정해야 하는 경우에는 세포 세척이나 원심분리 단계가 필요 없는 homogeneous assay가 가장 효율적이며, 시약 준비 및 반응 시간이 최소화되어야 합니다. 흡광, 형광 또는 발광 신호의 안정성(signal stability) 또한 중요한 요소입니다. 신호가 일정하게 유지되면 데이터를 기록할 수 있는 시간적 여유와 유연성이 생기며, plate를 대량으로 처리할 때 발생할 수 있는 데이터 변동성도 줄일 수 있습니다. 수천 개의 샘플을 스크리닝해야 하는 경우에는 고밀도 plate(384-well 또는 1536-well plate) 포맷으로 miniaturization이 가능한 고감도 분석법을 선택하는 것이 유리합니다.
Promega는 plate reader 기반의 cell health assay 제품군을 폭넓게 제공하고 있습니다. 이 제품군은 빠르고 민감도가 높으며, 사용이 간편하고 high-throughput에 적합하도록 설계되어 있습니다(2). 대부분의 homogeneous assay는 시약을 넣고 혼합한 후 측정하는 간단한 방식(add-mix-measure)이지만, 일부 실험에서는 샘플 이동(transfer), 반응(incubation) 또는 교반(agitation) 과정이 추가로 필요할 수 있습니다. 따라서 분석법을 선택하기 전에는 프로토콜 전체를 미리 꼼꼼히 검토하여 해당 워크플로우가 실험 목적에 적합한지 확인하는 것을 권장합니다.
연구 목적에 맞는 최적의 assay를 찾아보세요.
아래를 클릭하여 cell viability, cytotoxicity 그리고 apoptosis 측정을 위해 설계된 Promega의 다양한 plate 기반의 분석법을 비교해볼 수 있습니다.
어느 정도의 민감도가 필요한가요?
Assay를 선택할 때 고려해야 할 또 다른 요소는 검출 민감도(sensitivity)입니다. 실험에 요구되는 민감도는 일반적으로 샘플당 사용하는 세포 수와 밀접하게 관련되어 있습니다. 일반적으로 형광이나 흡광 기반의 분석보다 발광 기반의 분석이 더 높은 민감도를 가지는데, 이는 background 발광이 거의 없어 signal-to-noise ratio가 높기 때문입니다. 반면, 형광 기반 검출은 세포 자체의 고유 형광, 시약 또는 화합물의 형광, 그리고 excitation과 emission의 파장 간 스펙트럼 중첩(spectral overlap) 등으로 인해 signal-to-background ratio가 감소할 수 있습니다.
ATP 농도나 MTS tetrazolium 환원과 같은 세포 대사 지표를 측정하는 경우, 세포 유형에 따라 검출 민감도는 달라질 수 있습니다. 일부 assay는 incubation 시간을 늘리는 것만으로도 signal-to-background ratio를 개선할 수 있습니다. 검출 시약의 민감도는 plate 형태나 well당 세포 수 같은 모델 시스템의 변수뿐 아니라, 세포 생존율 감소와 같은 평가 파라미터에 따라서도 달라집니다. 예를 들어, 10,000개의 세포 집단에서 생존율 변화를 측정하려는 경우에는 가장 민감한 분석 기술이 반드시 필요한 것은 아닙니다. 예를 들어, CellTiter 96® Non-Radioactive Cell Proliferation Assay (Cat.# G4000)는 10,000개와 8,000개의 생존 세포 간의 차이를 쉽게 검출할 수 있습니다. 반대로, 소량의 세포를 사용하는 고밀도의 multiwell plate 형태를 사용하는 모델 시스템에서는 최고 수준의 검출 민감도가 요구될 수 있습니다. 이 경우에는CellTiter-Glo® Luminescent Cell Viability Assay(Cat.# G7570)처럼 100개 미만의 세포도 검출 가능한 고감도 분석이 적합합니다.
시약은 얼마나 안정적인가요?
자동화된 high-throughput screening(HTS) 플랫폼을 사용하는 연구자들에게는 시약의 안정성과 자동화 시스템과의 호환성이 중요한 고려사항입니다. Assay 시약은 여러 개의 plate에 분주하는 동안 상온에서 충분한 시간 동안 안정성을 유지해야 하며, assay로 생성된 신호 또한 장시간 동안 안정하게 유지되어야 데이터 측정을 연속적으로 또는 일괄 처리(batch mode) 방식으로 유연하게 진행할 수 있습니다. CellTiter-Glo® 2.0 Cell Viability Assay는 이러한 요구를 충족하도록 설계되어, 상온에서 수일간 보관이 가능하며, 생성된 발광 신호는 반감기가 길어 일괄 처리에도 적합할 만큼 안정적으로 유지됩니다.
어떤 장비가 필요한가요?
경우에 따라 흡광, 형광 또는 발광을 감지할 수 있는 장비의 보유 여부가 assay 선택에 영향을 줄 수 있습니다. Promega의 포트폴리오는 주요 cell health 분석법(viability, cytotoxicity 또는 apoptosis)에 대해 검출 방식을 선택할 수 있는 다양한 assay 형태를 제공합니다. 또한, CellTiter-Glo®Luminescent Cell Viability Assay (Cat.# G7570)와 같은 일부 assay는luminometer는 물론, CCD 카메라를 사용하는 장비에서도 결과를 측정할 수 있어 장비 선택에 유연성을 제공합니다.
나에게 꼭 맞는 장비를 찾아보세요.
GloMax® Microplate Reader는 사용이 간편하고 모듈형으로 설계된 검출 시스템으로, plate 기반 실험을 보다 유연하게 설계할 수 있도록 도와줍니다. Promega의 다양한 assay와 완벽하게 호환되며, 미리 탑재된 프로토콜 덕분에 간편하고 빠른 검출이 가능합니다.
어떤 plate를 사용해야 하나요?
Promega의 plate 기반 assay를 사용할 때는 연구 목적에 따라 적합한 plate 종류를 선택하는 것이 중요합니다. 세포를 현미경으로 관찰해야 하는 경우에는, 투명한 바닥(transparent bottom)을 가진 벽면이 불투명한(opaque) plate를 사용해야 합니다. 일반적으로, 형광 기반 assay에는 background 신호를 줄이기 위해 불투명한 black plate를 사용하며, 발광 기반 assay에는 빛의 강도를 극대화하기 위해 불투명한 white plate를 사용합니다. 하지만 대부분의 발광 assay는 신호 세기가 충분히 강력하기 때문에, black plate를 사용해도 문제가 없습니다. 특히 black plate는 형광과 발광 assay를 하나의 샘플에서 multiplexing할 때 유연성을 제공합니다. 흡광 assay의 경우 clear plate를 사용할 수 있지만, 형광이나 발광 assay에는 적합하지 않습니다. 적절한 plate와 장비의 조합은 신호 간 간섭 이나 데이터 왜곡 등의 문제를 줄이는 데 도움이 됩니다.
하나의 샘플로 여러 가지 assay를 수행하고 싶으신가요? (Multiplex 분석)
하나의 샘플에서 둘 이상의 assay를 수행하는 multiplex 분석은 다양한 정보를 동시에 얻을 수 있는 효율적이고 유연한 접근 방식입니다. 예를 들어, 하나의 well에서 세포 스트레스 반응 경로와 세포사멸 기전을 동시에 측정하거나, cell viability와 reporter 반응을 함께 측정해 결과를 생존 세포 수를 기준으로 normalization 할 수도 있습니다. Multiplex 분석을 수행하기 위해서는 사용하는 assay 시약 간의 화학적 반응 조건이 서로 호환 가능해야 하며, 서로 다른 검출 파장을 사용하거나 또는 형광과 발광 같은 서로 다른 검출 방식을 구분할 수 있는 능력이 필요합니다. Assay 간의 화학적 호환성이 확보된 경우에는, 하나의 샘플 well에서 동시에 multiplex 분석을 수행할 수 있습니다. 일부 조합의 경우에는 순차적으로 측정해야 합니다. 또 다른 경우에는 샘플 일부를 별도의 용기로 옮겨 분석을 수행할 수 있으며, 이러한 방법은 assay 간 화학적 비호환성, 장비 요구 사항 또는 plate 형식(예: 투명 vs. 불투명 플라스틱)의 제약을 극복하는 데 유용합니다. 예를 들어, LDH-Glo™ Cytotoxicity Assay (Cat.# J2380)는 소량의 배지 상층액을 불투명한 white plate로 옮겨 측정함으로써, 원래 세포가 들어 있던 plate는 reporter gene 분석, 이미징, 핵산 분석 등 다른 downstream assay에 그대로 활용할 수 있습니다.
하나의 샘플 well 내에서 multiplex 분석을 수행하면, 서로 다른 분석을 위해 여러 개의 병렬 샘플을 준비할 필요가 없어집니다. 이로 인해 시간, 노력, 비용을 절약할 수 있을 뿐만 아니라, 병렬 샘플을 사용할 때보다 통계적인 측면에서도 이점을 얻을 수 있습니다. Promega의 다양한 homogeneous 형태의 세포 독성, 세포사멸, 세포 생존력 assay는 배지를 옮길 필요 없이 동일한 샘플 well에서 multiplex 분석이 가능하도록 설계되어 있어, 연구자가 하나의 샘플에서 다양한 생물학적 파라미터를 동시에 측정할 수 있도록 도와줍니다.
Assay 결과는 재현성이 있나요?
데이터의 재현성(reproducibility)은 상용화된 assay를 선택할 때 중요한 고려 요소입니다. 하지만 대부분의 세포 기반 분석법에서는 반복 샘플 간의 변동성(variation)의 주요 원인은 시약 자체의 화학 반응(assay chemistry)보다는 세포에 의해 발생하는 경우가 많습니다. 세포를 분주하는 과정에서 발생하는 차이도 개별 세포로 균일하게 부유하지 않고 뭉치려는 경향이 있는 세포주를 사용할 경우에는 그 변동이 더욱 크게 나타날 수 있습니다. 또한 긴 incubation 시간이나 plate의 edge effect도 반복 샘플 간의 재현성을 떨어뜨리고, Z'-factor와 같은 품질 지표를 낮출 수 있습니다. 따라서 assay를 선택할 때는 단순히 시약의 성능뿐 아니라, 결과에 영향을 줄 수 있는 다양한 변동 원인을 이해하는 것이 중요합니다.
비용은 어느 정도인가요?
일반적으로 시약의 비용은 assay의 품질이나 사용자 편의성과 일정 부분 상충하는 경우가 많습니다. 비용이 저렴한 시약은 대체로 실험 과정이 복잡하거나, 민감도가 낮고, incubation 시간이 길어 세포에 독성을 유발할 수 있으며, 실험 시간도 더 오래 걸리는 경우가 많습니다. 그럼에도 불구하고 일부 연구 목적이나 조건에서는 비용이 낮은 assay가 적절할 수 있습니다. 다만, 세포 독성을 일으키는 시약은 실험 결과에 영향을 줄 수 있고, 다른 assay와의 multiplexing 적용을 제한할 수 있으므로 신중하게 선택해야 합니다.
반면, 품질 관리가 이루어진 상용 시약이나 assay 키트는 초기 비용은 높을 수 있지만, 재현성이 낮아 반복 실험을 해야 하는 상황을 줄여주어 결과적으로 시간과 자원을 절약할 수 있습니다. 예를 들어, ATP cell viability assay는 다른 assay에 비해 시약 비용은 다소 높을 수 있지만, 빠른 분석 속도(시간 절약), 높은 감도(세포 샘플 절약), 우수한 정확도(데이터 신뢰도 향상)를 고려하면 초기 비용을 상쇄할 수 있는 충분한 장점이 있습니다. 또한, 검출 감도가 우수하고 384-well 또는 1536-well 형태로 쉽게 축소하여 적용할 수 있는 assay는 세포 배양에 필요한 시약 사용량을 줄여줄 뿐 아니라, 고가이거나 희귀한 샘플(예: primary cell)도 소량으로 분석할 수 있어 비용 효율성이 매우 높습니다. 더불어, 실시간 측정이 가능한 assay는 시간 경과에 따른 데이터를 얻기 위해 여러 plate를 반복해서 준비할 필요가 없어, 실험 시간을 단축하고 전체 비용도 절감할 수 있습니다.
결론
Cell health 분석을 위한 실험을 계획하고 설계하는 데에는 다양한 옵션이 존재합니다. Cell viability또는 cytotoxicity assay를 선택하는 일은 쉽지 않지만, Promega는 연구 목표에 부합하는 다양한 솔루션과 리소스를 통해 그 선택을 돕고 있습니다. 추가적인 안내가 필요하신 경우, 아래의 Related Resources를 참고해 주세요. 또한 보다 구체적인 기술 지원이 필요하신 경우, Promega의 숙련된 Technical Services Scientists가 여러분의 실험이 성공적으로 진행될 수 있도록 도와드립니다.
References
1. Riss, T.L. and Moravec, R.A. (2004) Use of multiple assay endpoints to investigate the effects of incubation time, dose of toxin, and plating density in cell-based cytotoxicity assays. Assay Drug Dev Technol. 2(1), 51–62.
2. Zhang, J.H., Chung, T.D. and Oldenburg, K.R. (1999) A simple statistical parameter for use in evaluation and validation of high throughput screening assays. J Biomol Screen. 4(2), 67–73.
MyGlo™ Reagent Reader
Gold-standard 발광 기반의 cell viability 분석을 더욱 빠르고 간편하게, 개인용 96-well plate reader로 구현해보세요.