단백질 정제 방법
GST, His-tag, HaloTag, biotin 등의 affinity purification tag와 단백질 complex 정제를 위한 pull-down system을 포함한 단백질 정제 기술에 대한 가이드
가이드에 언급된 제품 주문 정보는 단백질 정제(Protein Purification) 제품 페이지를 참조하세요.
단백질 정제 소개
관심 단백질의 정제는 개별 단백질 연구를 위한 기본적인 단계입니다. 단백질 정제의 기본적인 4단계는 다음과 같습니다. 1) cell lysis, 2) matrix와 단백질 binding, 3) washing 및 4) elution. Cell lysis는 non-enzymatic 방법 (예. sonication 또는 French press), lysozyme와 같은 가수 분해 효소, FastBreak™ Cell Lysis Reagent와 같은 detergent 시약 등의 여러 가지 방법으로 진행할 수 있습니다. Native 단백질을 정제하는 것은 어려울 수 있기 때문에, affinity purification tag를 관심 재조합 단백질에 fusion 하여 단백질을 capture 하거나 검출하는 데 사용합니다.
여기에서는 정제 방법 선택 가이드라인과 affinity tag를 사용한 단백질 정제 프로토콜 예시를 포함하는 단백질 정제 전략에 대한 개요를 설명하고자 합니다.
단백질 정제 전략
단백질은 세포가 구조와 기능적으로 온전함을 유지하게 하는 생물학적 거대분자이며, 다수의 질병이 단백질 기능 이상(protein malfunction)과 관련됩니다. 단백질 정제는 개별 단백질 및 단백질 complex를 분석하고 다른 단백질, DNA 또는 RNA와의 interaction을 확인하기 위한 기본 단계입니다. 원하는 사이즈, throughput, downstream application에 따른 다양한 단백질 정제 전략이 존재합니다. 최적의 접근법은 경험적으로 결정해야 하는 경우가 많습니다.
단백질 정제
가장 적합한 단백질 정제 프로토콜은 정제하는 단백질뿐 만 아니라 재조합 단백질을 발현하는 데 사용되는 세포(예. 원핵세포 vs. 진핵세포) 등 다른 여러 가지 요소에 의해서 결정됩니다. 사용 편의성, 세포의 빠른 성장 속도, 낮은 배양 비용으로 인해 재조합 단백질을 생산하는 많은 연구자들은 여전히 Escherichia coli를 첫 번째 옵션으로 선택하고 있습니다. E. coli에서 발현된 단백질은 비교적 많은 양을 정제할 수 있지만, 이러한 단백질(특히 진핵생물의 단백질)은 적절한 단백질 활성이나 folding이 나타나지 않을 수 있습니다. 배양된 mammalian 세포는 적절한 post-translational modification을 통해 올바르게 folding 되고 기능적 성질을 지닌 mammalian 단백질을 생산하는 데 있어 더 나은 선택지가 될 수 있습니다(Geisse et al. 1996). 그러나 배양된 mammalian 세포의 재조합 단백질의 발현율이 낮기 때문에 정제에 어려움이 있습니다. 따라서 만족스러운 수율(yield)과 순도(purity)를 얻으려면 정제되지 않은 cell lysate로부터 관심 단백질을 매우 선택적이고 효율적으로 capture 해야 합니다.
정제를 단순화하기 위해 affinity purification tag를 관심 재조합 단백질에 fusion할 수도 있습니다(Nilsson et al. 1997).일반적인 fusion tag는 재조합 단백질의 N- 또는 C-말단에 추가되는 polypeptide, 저분자 단백질 또는 효소입니다. 서로 다른 tag의 생화학적 특성은 tag가 부착된 단백질의 안정성, 용해도 및 발현에 영향을 줍니다(Stevens et al. 2001). Fusion tag가 포함된 발현 vector를 사용하면 재조합 단백질 정제를 용이하게 할 수 있습니다.
단백질 complex 분리
Proteomics의 중요한 목표는 단백질 기능과 주요 세포 내의 과정을 담당하는 복잡한 네트워크의 구성을 규명하는 것입니다. Protein:protein interaction 분석을 통해 이러한 과정에 관여하는 세포 신호 전달 체계(cell signaling cascade)에 대한 의미 있는 통찰을 얻을 수 있으며, protein:nucleic acid interaction 연구를 통해 mRNA 조절, chromosomal remodeling 및 전사와 같은 생물학적 과정에 대한 중요한 정보를 밝혀낼 수도 있습니다. 예를 들어, transcription factor는 염색체의 특정한 인식 부위, 주로 유전자의 promoter에 결합하고 핵 내의 다른 단백질과 interaction 하여 전사 조절에 있어 중요한 역할을 합니다. 이러한 조절은 cell viability, 분화 및 성장에 필수적입니다(Mankan et al. 2009; Gosh et al. 1998).
Protein:protein interaction 분석은 단백질 구조 또는 기능을 저해하지 않으면서 고체 표면(solid surface)에 단백질을 적절한 방향으로 고정(immobilization) 하는 간단한 방법이 필요한 경우가 많습니다. 이러한 고정은 결합 능력을 간섭하지 않아야 하며 affinity tag를 사용하여 디자인할 수 있습니다. 단백질을 칩에 고정하는 방법은 protein:DNA interaction 및 protein:protein interaction을 분석하고 단백질 complex의 구성요소를 확인하는 데 많이 사용되는 접근 방법입니다(Hall et al. 2004; Hall et al. 2007; Hudson and Snyder, 2006). Functional protein microarray에는 일반적으로 고체 표면에 결합된 full-length단백질 또는 단백질 도메인(protein domain)이 포함됩니다. 형광 표지된 DNA는 array probe로 사용하며 이는 특정 probe에 결합하는 단백질을 확인하는 데 사용됩니다. Protein microarray는 protein:DNA interaction을 high-throughput 방식으로 확인할 수 있습니다. 또한 고정된 단백질을 protein pull-down assay에 사용하면 in vivo (mammalian 세포) 또는 in vitro에서 단백질 결합 파트너를 분리할 수 있습니다. 질량분석법(mass spectrometry)과 같은 downstream application에서는 단백질 결합 파트너 및 단백질 complex의 각각의 구성요소를 확인하기 위해 단백질 고정이 필요하지 않습니다.
단백질 정제를 위한 Affinity Tag
특정 단백질을 분리하거나 고정하는 한 가지 방법은 affinity tag를 사용하는 것입니다. 다양한 affinity tag가 개발되었으며(Terte, 2002) fusion tag는 재조합 단백질의 N- 또는 C-말단에 추가되는 polypeptide, 저분자 단백질 또는 효소입니다.
Polyhistidine
가장 일반적으로 사용되는 tag는 polyhistidine tag입니다(Yip et al. 1989). Polyhistidine tag를 사용한 단백질 정제는 니켈(nickel)과 같은 고정된 금속에 대한 histidine 잔기의 affinity에 의해 분리됩니다(Yip et al. 1989; Hutchens and Yip, 1990). 이러한 affinity interaction은 polypeptide의 imidazole 부위에 질소가 금속 이온의 빈 배위 결합 자리에 결합한 결과로 여겨집니다. 금속은 지지체(support)에 공유 결합된 chelate와의 complex 형성을 통해 지지체에 고정됩니다.
Polypeptide tag는 단백질 정제에 있어 여러 가지 이점을 제공합니다. Polypeptide tag는 크기가 작기 때문에 크기가 큰 다른 tag보다 면역원성이 낮습니다. 그래서 일반적으로 정제 후 downstream application에 이용하기 위해 tag를 제거할 필요가 없습니다. Polyhistine tag는 관심 단백질의 N- 또는 C-말단에 붙일 수 있습니다. 마지막으로, polyhistidine tag와 금속의 interaction은 tag의 3차 구조에 의존적이지 않기 때문에 denaturing 조건에서 insoluble 단백질을 정제할 수 있습니다.
Glutathione-S-Transferase
Affinity tag인 glutathione-S-transferase (GST)는 고정된 glutathione-covered matrix에 대한 GST의 강한 affinity를 기반으로 정제합니다(Smith and Johnson, 1988). Glutathione-S-transferase는 진핵생물에 존재하는 multifunctional cytosolic protein의 일종입니다(Mannervik and Danielson, 1988; Armstrong, 1997). 일반적으로 GST isoform은 박테리아에서 발견되지 않기 때문에 endogenous 박테리아 단백질은 정제 resin에 결합하기 위해 GST fusion protein과 경쟁하지 않습니다. 26kDa 크기의 GST affinity tag는 박테리아에서 발현되는 여러 진핵생물의 단백질 용해도를 향상시킵니다.
HaloTag® Protein Tag
단백질 fusion tag는 적절한 수준의 soluble 단백질 발현과 정체를 돕기 위해 사용됩니다. 독특한 단백질 tag인 HaloTag® 단백질은 E. coli에서 재조합 단백질의 발현과 용해도를 향상시킬 수 있도록 설계되었습니다. HaloTag® protein tag는 Rhodococcus rhodochrous dehalogenase에서 변형된 34kDa 크기의 monomeric protein tag입니다.
HaloTag® 단백질은 특유의 synthetic linker에 빠르게 공유결합하여 비가역적으로 결합하도록 디자인되었습니다. Synthetic linker는 형광 dye 및 고체 지지체와 같은 다양한 개체에 부착하여 발현 스크리닝을 위해 cell lysate에서 fusion 단백질을 표지하고 purification resin에서 fusion 단백질을 capture할 수 있습니다.
HaloTag® 기술은 다양한 단백질 발현 시스템과 호환되며 E. coli, mammalian 세포 및 cell-free 시스템에서 발현된 단백질에 적용할 수 있습니다.
HaloTag® 기술
HaloTag는 단백질 정제, localization, trafficking 및 turnover를 비롯하여 단백질 interaction 및 초고해상도 현미경을 사용한 application에 적용할 수 있는 강력한 기술입니다.
Mammalian 세포에는 endogenous HaloTag® 단백질이 없기 때문에 false positive 또는 비특이적 interaction이 측정될 가능성이 최소화됩니다. 공유결합을 통한 capture 방법과 빠른 결합 속도(binding kinetic)의 조합이 기존의 affinity tag와 관련된 equilibrium 기반의 한계를 극복하고 낮은 발현 상태에서도 효율적인 단백질 capture가 가능합니다. 또한 안정성이 높은 HaloTag® protein:ligand interaction을 통해 SDS-PAGE 분석 전에 단백질 complex를 SDS sample buffer에서 boiling할 수 있습니다.
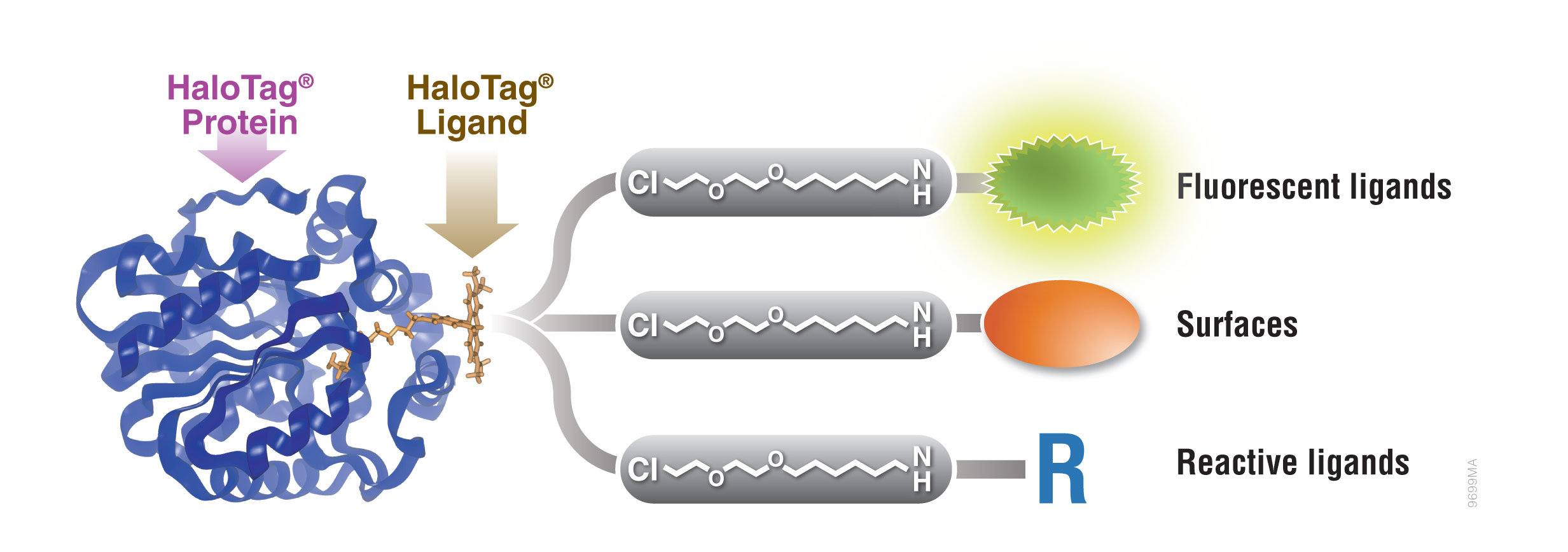
Figure 1. HaloTag® protein tag의 interchangeable 기능. 일반적인 생리학적 조건에서 HaloTag® fusion 단백질과 HaloTag® Ligand의 reactive linker와의 공유결합이 형성됩니다. 이 interaction은 매우 특이적이며 비가역적입니다. 서로 다른 기능의 다양한 HaloTag® Ligand를 사용할 수 있어 새로운 발현 construct를 디자인하고 만들 필요가 없습니다.
Magnetic resin을 이용한 Polyhistidine-Tagged 단백질의 빠른 정제
Magnetic resin을 이용한 Polyhistidine-Tagged 단백질의 빠른 정제
High-throughput으로 단백질을 정제하는 방법에 대한 수요가 증가하고 있습니다. Magnetic resin을 사용하면 여러 번의 원심분리 단계를 거치지 않고 여러 개의 튜브에 샘플을 순차적으로 옮길 필요 없이 affinity tagged 단백질 정제가 가능합니다. 우수한 단백질 purification resin을 정의하는 기준은 비특이적 단백질 binding 최소화, fusion protein에 대한 높은 결합력 및 fusion 단백질의 효율적인 회수입니다. MagneHis™ Protein Purification System은 이러한 기준을 충족하여 광범위한 분자량과 다양한 발현 수준의 단백질을 정제할 수 있습니다. 결합 입자의 자성으로 인해 하나의 튜브에서 crude cell lysate로부터 단백질을 정제할 수 있습니다. 또한 이 시스템은 high-throughput application에서 자동화된 liquid-handling 플랫폼과 함께 사용할 수 있습니다.
MagneHis™ Protein Purification System
MagneHis™ Protein Purification System은 paramagnetic 전하를 띠는 니켈 입자 (MagneHis™ Ni-Particles)를 사용하여 crude cell lysate에서 직접 polypeptide tagged 단백질을 분리합니다. Figure 2는 MagneHis™ Protein Purification System 프로토콜의 모식도를 보여줍니다. Polyhistidine-tagged 단백질은 1ml 미만의 배양액에서 소규모로 정제하거나 1L 이상의 배양액에서 대규모로 정제할 수 있습니다. Beckman Coulter Biomek® FX 또는 Tecan Freedom EVO® instrument와 같은 liquid handler 플랫폼을 사용하여 high-throughput으로 샘플을 처리할 수 있습니다. Polyhistidine-tagged 단백질은 native 또는 denaturing (2~8M urea 또는 guanidine-HCl) 조건에서 정제할 수 있습니다. Mammalian 및 insect 세포 배양 배지에 serum이 포함되어 있어도 단백질 정제에 영향을 주지 않습니다. 추가 정보 및 자세한 프로토콜은 Technical Manual #TM060 및 MagneHis™ Protein Purification System Automated Protocol을 참조하세요.
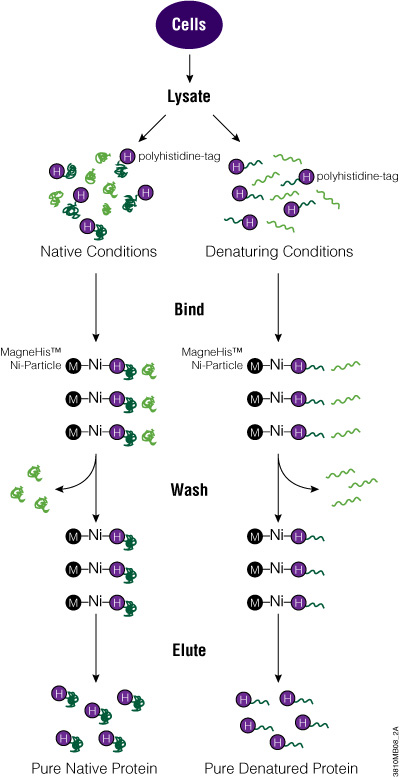
Figure 2. MagneHis™ Protein Purification System 프로토콜 모식도
프로토콜: MagneHis™ Purification system을 이용한 박테리아 세포에서 발현된 단백질의 정제
필요한 Material:
- MagneHis™ Protein Purification System및 프로토콜
- 플라스크 또는 튜브용 37°C incubator
- Shaker
- Magnetic separation 스탠드
- 1M imidazole solution (pH 8.0; insect 또는 mammalian cell 또는 배양 배지 샘플 정제용)
- 추가 binding/wash buffer (많은 수의 insect cell, mammalian cell, 또는 배양 배지 샘플을 처리하는 경우 필요할 수 있음)
- Solid NaCl (insect 또는 mammalian cell 또는 배양 배지 정제용)
Denaturing 조건에서 정제. 박테리아 세포에서 발현되는 단백질은 insoluble inclusion body 형태로 존재할 수 있습니다. 단백질이 inclusion body에 존재하는지 확인하려면 Technical Manual #TM060에 설명된 대로 FastBreak™ Cell Lysis Reagent, 10X를 사용하여 lysis 단계를 수행합니다. 원심분리를 통해 cellular debris을 pellet으로 만들고, supernatant와 pellet을 gel 분석을 통해 polypeptide tagged 단백질이 어디에 존재하는지 확인합니다.
Insoluble 단백질을 효율적으로 분리하기 위해서는 denaturing 조건에서 정제해야 합니다. Polyhistidine-tagged fusion 단백질과 MagneHis™ Ni-Particle의 interaction은 3차 구조에 의존적이지 않으므로 2~8M guanidine hydrochloride 또는 urea와 같은 강력한 denaturant를 세포에 첨가한 denaturing 조건에서 fusion 단백질을 capture 하고 정제할 수 있습니다. 단백질이 aggregation 되지 않도록 전체 실험 과정은 denaturing 조건에서 진행해야 합니다. Promega는 고체 형태의 guanidine-HCl 또는 urea를 MagneHis™ Binding/Wash 및 Elution Buffer에 직접 첨가하여 denaturing buffer를 준비하는 것을 권장합니다. 자세한 정보는 Technical Manual #TM060을 참조하세요.
Note: FastBreak™ Cell Lysis Reagent와 denaturant를 함께 사용하지 마세요. Urea 또는 guanidine-HCl과 같은 denaturant를 사용하여 세포를 직접 lysis할 수 있습니다.
Insect 및 mammalian 세포에서 단백질 정제. 2 × 106cells/ml cell density에서 진행합니다. 조직 배양 용기에 부착된 세포를 긁어내고 이 세포 개수로 배양 배지에 resuspension합니다. 최대 10% serum이 함유된 배양 배지에서 세포를 처리할 수 있습니다. 위에서 언급한 ml당 세포 수를 초과한 샘플에서 진행할 경우 단백질 수율이 감소하고 비특이적 결합이 증가할 수 있습니다. 세포 배양 배지에 분비된 단백질의 경우, 정제 전에 배지에서 모든 세포를 제거합니다. 자세한 정보는 Technical Manual #TM060을 참조하세요.
MagneHis™ System 프로토콜
MagneHis™ System 사용에 대한 자세한 정보와 세부 프로토콜은 Technical Manual #TM060에서 확인할 수 있습니다. Liquid handler에서 MagneHis™ System 자동화 프로토콜도 제공됩니다. (#EP011).
Column 또는 batch format으로 Polyhistidine-Tagged 단백질의 medium 및 large 스케일 정제
Resin 기반의 affinity tagged 단백질 정제에 사용되는 가장 일반적인 두 가지 지지체 물질은 agarose와 silica gel입니다. Silica는 크로마토그래피 지지체로서, swelling에 취약하지 않으며 분해나 변형 없이 압력과 유속(flow rate)의 큰 변화를 견딜 수 있는 견고한 기계적 구조(rigid mechanical structure)를 가지고 있다는 장점이 있습니다. Silica는 단백질과 같은 큰 생체 분자가 더 많이 결합할 수 있는 macroporous silica를 포함하여 다양한 pore 및 입자 크기로 제공됩니다. 그러나 affinity purification에 사용되는 silica 고체 지지체는 사용 가능한 시약 반응이 제한적이고 surface modification 효율이 상대적으로 낮다는 단점이 있습니다.
HisLink™ Protein Purification Resin(Cat.# V8821, V8823)은 silica 표면을 새롭게 변경하여 높은 결합력을 가진 tetradenate metal-chelated 고체 지지체를 제공하는 동시에 변형하지 않은 silica의 특성인 비특이적 결합을 제거함으로써 이러한 한계를 극복하였습니다. HisLink™ Resin은 높은 수준의 tetradentate-chelated nickel을 함유하도록 변형된 marcoporous silica resin입니다(>20mmol Ni/ml settled resin). Figure 3는 HisLink™ Resin과 polyhistidine의 interaction 모식도를 보여줍니다. HisLink™ Resin은 pore 크기가 크기 때문에 1ml resin당 35mg polyhistidine-tagged 단백질의 결합 용량을 제공합니다.
HisLink™ Resin은 박테리아에서 발현된 polyhistidine-tagged 단백질을 효율적으로 capture하고 정제할 수 있게 합니다. 이 resin은 IMAC (immobilized metal affinity chromatography) matrix가 필요한 일반적인 application에도 사용할 수 있습니다 (Porath et al. 1975; Lonnerdal and Keen, 1982). HisLink™ Resin은 column 또는 batch 정제 format으로 사용할 수 있습니다. 자세한 프로토콜은 Technical Manual #TB327을 참조하세요.
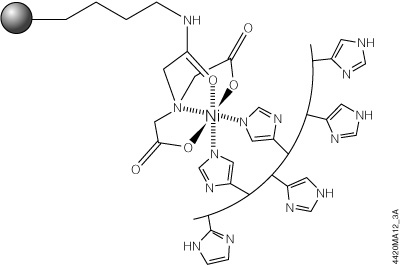
Figure 3. HisLink™ Resin과 Polyhistidine interaction의 모식도. Polyhistidine-tag가 결합할 수 있는 두 곳의 결합 부위는 polyhistidine-tagged polypeptide가 존재하는 경우 histidine과 빠르게 결합합니다.
HisLink™ Resin을 사용한 column 기반의 정제
HisLink™ Resin은 polypeptide tagged 단백질을 정제하기 위해 사용하는 전통적인 방법을 제공하며 적절한 충진제 부피(bed volume)로 패킹할 수 있는 column만 있으면 됩니다. 중력에 의한 유량(gravity-driven flow) 조건에서 1ml이 채워진 경우, HisLink™ Resin은 약 1ml/min 평균 유속을 나타냅니다. 일반적으로 resin 1~2mL/min 유속 조건이 polypeptide tagged 단백질을 효율적으로 capture 할 수 있는 최적의 조건입니다. 정제된 lysate를 HisLink™ column에 중력으로 흐르게 하면 polypeptide tagged 단백질을 완전히 capture 하고 효율적으로 elution 할 수 있습니다. 하지만 resin을 진공 여과 장치(예. Vac-Man® Vacuum ManifoldCat.#A7231)와 함께 사용하면 여러 개의 column을 동시에 처리할 수 있습니다. 또한 HisLink™ Resin은 FPLC와 같은 low – medium pressure 액체 크로마토그래피 시스템을 사용하는 affinity purification
HisLink™ Resin과 Gravity-Flow Column Chromatography를 사용하여 정제된 lysate에서 단백질을 정제하는 프로토콜 예시
필요한 material:
- HisLink™ Protein Purification Resin(Cat.# V8821) 및 프로토콜
- HEPES buffer (pH 7.5)
- imidazole
- HisLink™ Binding Buffer
- HisLink™ Wash Buffer
- HisLink™ Elution Buffer
- Column
Cell Lysis: Sonication, French press, bead milling, lytic enzyme (예. lysozyme) 처리 방법을 이용하거나 FastBreak™ Cell Lysis Reagent(Cat.# V8571)와 같은 상용화된 cell lysis reagent를 사용하여 세포를 lysis할 수 있습니다. Lysozyme을 사용하여 lysate를 준비하는 경우, binding buffer와 wash buffer에 salt(>300mM NaCl)를 첨가하여 lysozyme이 resin에 결합되지 않도록 해야 합니다. PMSF (1mM)와 같은 protease inhibitor를 cell lysate에 첨가해도 HisLink™ Resin과 polyhistidine tagged 단백질과의 결합이나 elution을 억제하지 않기 때문에 endogenous protease에 의해 타겟 단백질이 분해되는 것을 방지하기 위해 이러한 inhibitor를 첨가하는 것을 권장합니다. High-density 배양 세포에서 lysate를 준비할 때 DNase와 RNase (최대 20μg/ml 농도)를 첨가하면 lysate의 점성(viscosity)이 감소되어 정제 과정이 수월해질 수 있습니다.
- HisLink™ Binding Buffer, Wash Buffer, Elution Buffer를 준비합니다.
Note: Polyhistidine-tagged 단백질은 250~1,000mM imidazole을 사용하여 elution 할 수 있습니다. 6개 미만의 histidine을 함유한 polyhistidine tag는 일반적으로 elution에 필요한 imidazole이 적은 반면, 6개 이상의 polyhistidine을 함유한 polyhistidine 단백질은 더 많은 양의 imidazole이 필요할 수 있습니다. - 타겟 단백질을 정제하는 데 필요한 column 부피를 결정합니다. 대부분의 경우 침전된 resin 1ml이면 최대 1L의 배양액에서 일반적으로 발견되는 단백질의 양을 정제하기에 충분합니다(cell density O.D.600 < 6.0). 발현 수준이 매우 높은 경우(예: 50mg protein/L), 배양액 1L당 최대 2mL resin이 필요할 수 있습니다.
- 필요한 침전 resin의 부피를 결정한 후에 동일한 양의 물을 column에 피펫팅하여 넣고 물의 상단부분에 표시하여 이 양을 column에서 직접 사전 보정(precalibration) 합니다. 이 표시는 침전된 resin의 충진 부피 상단을 나타냅니다. Column에 resin을 첨가하기 전에 물을 제거합니다.
- Resin이 완전히 suspension 되었는지 확인하고 피펫을 사용하여 column에 표시된 선에 맞춰 resin을 column에 채웁니다. Resin이 침전될 때까지 기다린 후 필요에 따라 resin을 첨가하거나 제거하여 resin의 부피를 조정합니다.
Note: 혼합 후 10~15초 이내에 resin을 피펫팅하여 섞지 않으면 상당한 침전이 발생하므로 resin을 resuspension 할 필요가 있습니다. 또는 이동 중에 resin을 suspension상태로 유지하기 위해 magnetic stir bar를 사용할 수 있습니다. Resin이 손상되는 것을 방지하려면 resin을 피펫으로 옮기는 데 필요한 시간보다 더 오래 교반하지 마세요. - Column의 내용물을 따라내고 5배 column 부피만큼의 binding buffer로 resin을 평형상태로 만들어 buffer가 resin의 충진 부피를 완전히 채웁니다.
- Cleared lysate가 column을 완전히 채울 때까지 resin에 조심스럽게 첨가합니다. 1ml의 column 부피 당 column을 통과하는 유속이 1~2mL/분을 초과해서는 안 됩니다. 일반적인 중력에 의한 유량(gravity flow) 조건에서 유속은 일반적으로 약 1ml/분입니다. 실제 유속은 사용하는 column의 유형과 lysate의 clear와 여과 정도에 따라 달라집니다. Lysate를 column에 추가한 이후에는 resin이 건조되지 않도록 합니다.
- 최소 10~20배의 column 부피만큼의 wash buffer를 사용하여 resin에 결합되지 않은 단백질을 washing합니다. Wash buffer 전체를 2~3 개로 분주하고 분주한 각각의 buffer가 resin 충진 부피를 완전히 채워지도록 기다린 후 다음 분주 buffer를 추가합니다.
- Wash buffer가 resin 충진 부피 상단을 완전히 채우면 elution buffer을 추가하고 특정 fraction (0.5~5ml fraction)을 collection합니다. Elution 프로파일은 단백질에 의존적이지만, polyhistidine-tagged 단백질은 일반적으로 첫 1ml에서 elution됩니다. Imidazole 농도가 타겟 단백질을 효율적으로 elution할 수 있을 정도로 높은 경우, 일반적으로 침전된 resin 1.0ml당 3~5ml buffer를 collection하면 elution 과정이 완료됩니다.
HisLink™ Resin를 사용한 batch 단백질 정제
HisLink™ Resin의 주요 장점 중 하나는 batch 정제에 사용할 수 있다는 점입니다. Batch 방식에서, 타겟 단백질은 4~22°C에서 약 30분 동안 lysate와 resin이 혼합되는 과정을 통해 resin에 결합됩니다. 단백질과 결합된 resin은 컨테이너 바닥에 침전되면 사용한 lysate는 제거합니다. Washing 과정은 적절한 wash buffer에 resin을 resuspension 하고 resin이 침전될 수 있도록 잠시 기다리면 됩니다. 그런 다음 wash buffer를 조심스럽게 따라냅니다. 이 과정을 원하는 횟수만큼 반복합니다. 최종 elution은 HisLink™ Resin를 column으로 옮겨 단백질을 fraction 별로 elution 하는 것이 가장 좋습니다. Batch 정제의 장점은 다음과 같습니다. 1) 정제에 소요되는 시간이 더 짧습니다. 2) 다량의 lysate를 처리할 수 있으며 3) 정제 전에 lysate를 clearing할 필요가 없습니다.
FPLC를 통한 Polyhistidine-Tagged 단백질 정제
Silica 기반의 견고한 입자 구조(rigid particle structure)를 가지는 HisLink™ Resin은 resin에 lysate를 채우거나, resin에서 단백질을 washing 또는 elution하기 위해 압력을 가해야 하는 application에 적합합니다. 이와 같은 application에는 양압 또는 음압(예. FPLC 및 진공 시스템)에서 작동하는 수동 및 자동 시스템이 모두 포함됩니다. 자동화 플랫폼에서 HisLink™ Resin 사용을 시연하기 위해, GE Healthcare AKTA Explorer를 사용하여 1L의 배양액에서 밀리그램 단위의 polypeptide tagged 단백질을 정제했습니다. 이 배양액은 binding/wash buffer 20ml에 lysis하고 HisLink™ Resin 1ml이 포함된 column에 로딩했습니다. 회수된 단백질의 총량은 본래의 lysate에서 발현된 단백질의 75~90%로 추정됩니다.
Denaturing 조건에서의 단백질 정제: Inclusion body로 발현되고 guanidine-HCl 또는 urea와 같은 chaotropic agent로 lysis된 단백질은 binding buffer, wash buffer, elution buffer에 적절한 양의 denaturant(최대 6M guanidine-HCl 또는 최대 8M urea)를 포함하도록 프로토콜을 변경하여 정제할 수 있습니다.
HisLink™ Resin은 column 또는 batch 정제 형식으로 사용할 수 있습니다. 자세한 프로토콜은 Technical Manual #TB327을 참조하세요.
HaloTag® Fusion 단백질 정제
Mammalian 세포에서 HaloTag® 단백질 정제
배양된 mammalian 세포는 적절한 post-translational modification을 통해 적절하게 folding된 기능적인 mammalian 단백질을 생산하는 데 적합한 환경을 제공합니다. 그러나 배양된 mammalian 세포에서 재조합 단백질의 발현 수준이 낮은 경우 문제가 발생합니다. 따라서 만족스러운 수율과 순도를 얻기 위해서는 crude cell lysate로부터 이러한 단백질을 선택적이고 더 효율적으로 정제해야 합니다. 대부분의 affinity tag 단백질 정제 방법에서 사용하는 평형상태에 기반한 결합은 (resin과의) 단백질 결합 및 결합되지 않은 단백질 상태가 지속적으로 전환된다는 것을 의미합니다. 이 평형상태는 tag의 단백질 농도 및 결합 친화도에 따라 달라집니다. 따라서 낮은 발현 수준에서는 결합 효율이 감소하여 fusion 단백질의 회수율이 낮아질 수 있습니다.
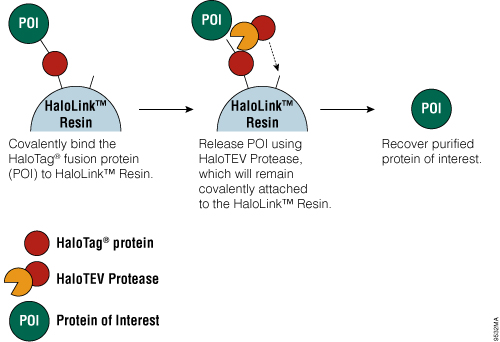
Figure 4. HaloTag® 기술을 사용한 단백질 정제 모식도.
HaloTag® Mammalian Protein Purification Systems (Cat.# G6795 및 Cat.# G6790)은 모든 단백질에 유전적으로 fusion되어 mammalian 세포에서 일시적으로 또는 안정적으로 발현될 수 있는 HaloTag® 단백질 tag를 사용합니다. 세포 lysis 이후, HaloTag® fusion 단백질은 HaloLink™ Resin에 공유결합으로 capture 되고 비특이적 단백질은 washing을 통해 제거합니다. 타겟 단백질은 HaloTag® 단백질 tag와 타겟 단백질을 연결하는 amino acid linker 서열에 포함되어 있는 최적화된 TEV protease 인식 부위에서 특이적인 proteolytic cleavage를 통해 방출됩니다. Protease를 제거하기 위한 2차 단계가 필요하지 않도록, HaloTag®(HaloTEV Protease; Cat.# G6601)에 fusion된 TEV protease를 사용하여 HaloTag® fusion 단백질을 digestion 한 다음 HaloLink™ Resin에 공유결합으로 capture 하여 정제 과정을 간소화할 수 있습니다. 이 간단한 정제 과정에서는 buffer를 교환할 필요 없이 전체 과정에 약한 생리학적 buffer를 사용합니다.
E. coli에서 HaloTag® Protein 정제
HaloTag® Protein Purification System (Cat.# G6280)은 E. coli에서 N-terminal HaloTag® fusion 단백질로 발현되는 단백질을 공유결합을 통해 효율적이고 특이적으로 capture 할 수 있도록 합니다. Mammalian 세포에서 단백질 정제에 적합한 HaloTag® 단백질 특성 중 대부분은 E. coli 세포에서의 단백질 정제에도 적합한 특성입니다. pFN18A HaloTag® T7 Flexi® Vector (Cat.# G2751)와 pFN18K HaloTag® T7 Flexi® Vector (Cat.# G2681)를 비롯해, HaloTag® 단백질 및 polyhistidine을 dual tag로 사용할 수 있는 non-Flexi® vector를 포함한 E. coli용으로 특이적으로 설계된 다양한 발현 vector를 사용하면 HaloTag® fusion 단백질을 E. coli에서 발현시킬 수 있습니다. 이러한 non-Flexi® vector, pH6HTN His6HaloTag® T7 Vector (Cat.#G7971) 및 pH6HTC His6HaloTag® T7 Vector (Cat.# G8031)를 사용하면 multiple cloning site를 사용한 기존 방식의 cloning이 가능합니다. 이러한 dual tag vector는 HaloTag® 단백질의 공유결합 능력을 유지하면서 HaloTag® fusion 단백질의 정제를 가능하게 합니다. HaloTag® Protein Purification System을 사용하면 형광 HaloTag® Ligand를 사용하여 단백질 발현 수준을 gel 내에서 검출 및 정량을 쉽게 수행할 수 있습니다.
HaloTag® Protein Purification System 프로토콜
HaloTag® Mammalian Protein Detection and Purification System에 대한 자세한 프로토콜은 Technical Manual, TM348을 참조하세요. E. coli에서의 HaloTag® 단백질 정제에 관한 프로토콜은 HaloTag® Protein Purification System Technical Manual, TM312를 참조하세요.
Biotinylated 단백질의 정제
SoftLink™ Soft Release Avidin Resin
Biotinylated fusion 단백질은 SoftLink™ Soft Release Avidin Resin을 이용한 affinity를 통해 정제할 수 있습니다. 독자적으로 개발된 이 resin은 exogenous biotin을 첨가하여 native 조건에서 fusion 단백질을 elution할 수 있습니다.
Avidin:biotin interaction은 매우 강력하기 때문에 avidin-conjugated resin에서 biotin-tagged 단백질을 elution하려면 일반적으로 denaturing 조건이 필요합니다. 반면, monomeric avidin을 사용하는 SoftLink™ Soft Release Avidin Resin은 nondenaturing 5mM biotin 용액으로 단백질을 elution할 수 있습니다. Monomeric avidin-biotin complex의 dissociation 속도는 충분히 빠르기 때문에 중성 pH 및 낮은 salt 농도 조건에서 결합된 모든 단백질을 효과적으로 회수할 수 있습니다.
SoftLink™ Soft Release Avidin Resin은 여러 화학 시약(예. 0.1N NaOH, 50mM acetic acid 및 nonionic detergent)에 대한 내성이 강하여 강력한 wash 조건에서도 사용할 수 있습니다.
SoftLink™ Soft Release Avidin Resin 프로토콜
SoftLink™ Soft Release Avidin Resin 프로토콜은 Product Information Sheet 9PIV201를 참고하세요.
단백질 Complex 정제를 위한 Pull-Down 방법
HaloTag® Pull-Down Assay
기존의 단백질 pull-down 접근법은 단백질과 affinity resin의 결합에 의존적이며, 이 과정은 보통 효율적이지 않습니다. 또한 HaloTag® Mammalian Pull-Down Systems은 관심 단백질과 affinity resin의 결합에 의존적이지만, HaloTag® protein fusion tag는 다른 여러 tag와는 달리 공유결합을 통해 resin에 비가역적으로 빠르게 결합합니다. 이러한 특성은 단백질 complex를 capture 하고, capture 후에 단백질 complex가 유지될 가능성을 높입니다. 또한 mammalian 세포에는 HaloTag® 단백질과 동일한 endogenous 단백질이 없기 때문에 위양성 또는 비특이적 상호작용을 검출할 가능성이 최소화됩니다. HaloTag® Mammalian Protein Pull-Down System의 프로토콜에 대한 개요는 Figure 5에 묘사되어 있습니다. HaloTag® Mammalian Pull-Down and Labeling System (Cat.# G6500)와 HaloTag® Mammalian Pull-Down System (Cat.# G6504)에 대한 추가 정보 및 자세한 프로토콜은 Technical Manual #TM342에서 이용할 수 있습니다. HaloTag® Complete Pull-Down System (Cat.# G6509)에 대한 정보는 Technical Manual #TM360에서 확인할 수 있습니다.
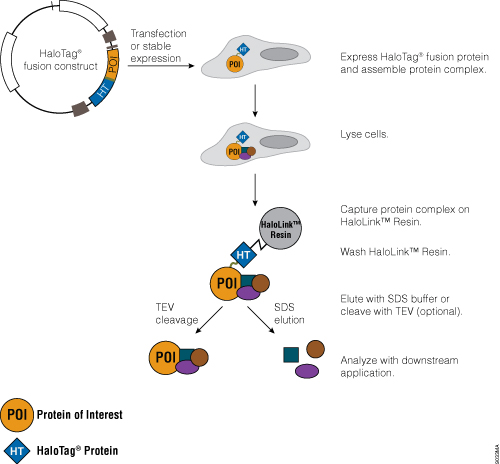
Figure 5. HaloTag® Mammalian Pull-Down System 프로토콜의 모식도
HaloTag® Pull-Down Assay 프로토콜
HaloTag® Pull-Down Assay에 대한 자세한 프로토콜은 HaloTag® Mammalian Pull-Down and Labeling System Technical Manual TM342 및 HaloTag® Complete Pull-Down System Technical Manual TM360을 참조하세요.
참고문헌
- Armstrong, R.N. (1997) Structure, catalytic mechanism, and evolution of the glutathione transferases. Chem. Res. Toxicol. 10, 2–18.
- Geisse, S. et al. (1996) Eukaryotic expression systems: A comparison. Protein Expr. Purif. 8, 271–82.
- Gosh, S. et al. (1998) NFκB and Rel proteins: Evolutionarily conserved mediators of immune responses. Annu. Rev. Immunol. 16, 225–60.
- Hall, D.A. et al. (2007) Protein microarray technology. Mech. Ageing Dev. 128, 161–7.
- Hall, D.A. et al. (2004) Regulation of gene expression by a metabolic enzyme. Science 306, 482–4.
- Hudson, M.E. and Snyder, M. (2006) High-throughput methods of regulatory element discovery. Biotechniques 41, 673–81.
- Hutchens, T.W. and Yip, T.T. (1990) Differential interaction of peptides and protein surface structures with free metal ions and surface-immobilized metal ions. J. Chromatogr. 500, 531–42.
- Lonnerdal, B. and Keen, C. (1982) Metal chelate affinity chromatography of proteins J. Appl. Biochem. 4, 203–8.
- Mankan, A.K. et al. (2009) NF-kappaB regulation: The nuclear response. J. Cell. Mol. Med. 13, 631–43.
- Mannervik, B. and Danielson, U.H. (1988) Glutathione transferases—structure and catalytic activity. CRC Crit. Rev. Biochem. 23, 283–337.
- Nilsson, J. et al. (1997) Affinity fusion strategies for detection, purification, and immobilization of recombinant proteins. Protein Expr. Purif. 11, 1–16.
- Porath, J. et al. (1975) Metal chelate affinity chromatography, a new approach to protein fractionation. Nature 258, 598–9.
- Smith, D.B. and Johnson, K.S. (1988) Single-step purification of polypeptides expressed in Escherichia coli as fusions with glutathione S-transferase. Gene 67, 31–40.
- Stevens, R.C. et al. (2001) Global efforts in structural genomics. Science 294, 89–92.
- Terpe, K. (2002) Overview of tag protein fusions: From molecular and biochemical fundamentals to commercial systems. Appl. Microbiol. Biotechnol. 60, 523–33.
- Yip, T.T. et al. (1989) Evaluation of the interaction of peptides with Cu(II), Ni(II), and Zn(II) by high-performance immobilized metal ion affinity chromatography. Anal. Biochem. 183, 159–71.