크기는 중요하다: NanoLuc® Technology가 바이러스학 연구를 진보시키다
Kyle Hooper
Promega Corporation
Publication Date: September 2018
t-pub 202
초록
재조합 reporter 바이러스는 동물 모델에서 바이러스의 병원성과 전파를 연구하기 위한 필수적인 도구입니다. 여기에서는 NanoLuc®, NanoBIT® 및 NanoBRET™ 기술을 사용하여 바이러스의 in vivo 수명 주기를 조사한 연구를 중점적으로 다루고자 합니다.
서론
2012년에 NanoLuc® luciferase(NLuc)라는 새로운 reporter와 검출 시약인 Nano-Glo® Luciferase Assay System가 소개되었습니다. NLuc은 분자적으로 진화된 19kDa의 심해 새우에서 유래된 luciferase로 안정성이 높아지고 밝기가 개선되었습니다. 원래 luciferase 기질인 coelenterazine은 화학적으로 진화하여 더 밝고 안정적인 기질인 furimazine으로 개발되었습니다. NLuc과 furimazine은 firefly luciferase (FLuc) 또는 Renilla luciferase (Rluc)보다 100배 이상 밝은 발광 signal을 생성합니다. 이에 비해 NanoLuc® 발광은 Gaussia와 같이 다른 작고 밝은 luciferase처럼 flash signal이 아닌 glow kinetics의 긴 signal lifetime을 나타냅니다. 또한, 다른 주요 기능으로 인해 NLuc은 이상적인 reporter입니다. 19kDa의 작은 NanoLuc® luciferase는 온도에 안정적이고, 광범위한 pH 범위에서 활성을 나타내며, PTM (post-translational modification)이 필요하지 않았습니다. NLuc은 460nm blue light를 생성합니다. NLuc과 Nano-Glo® Assay System의 개발, 특성 및 초기 application에 대한 자세한 내용은 Hall 등의 논문에서 확인할 수 있습니다(1).
NLuc의 blue light 발광은 동물 모델에서의 이미징에 어려움이 있으나, 발광의 밝기, 긴 발광 signal과 작은 크기로 인해 상당한 이점을 가지고 있습니다.
Luciferase는 재조합 reporter 바이러스를 만드는 중요한 도구로, 동물 모델에서의 바이러스 수명 주기와 치사력(lethality)을 잘 이해하는데 사용됩니다(2). Luciferase가 가진 어려움도 있지만, reporter가 발현되는 바이러스는 발광(bioluminescent) 이미징을 사용하여 시간에 따른 한 동물 내에서의 감염을 추척하기가 더 용이합니다. FLuc은 살아있는 동물에서 약 600nm에서 방출되기 때문에 in vivo동물 이미징에 가장 일반적으로 사용되며, 이는 심부 조직 이미징에 더 적합합니다. FLuc은 61 kDa으로 다소 크기가 큰 단백질이고 바이러스 캡시드(capside) 크기가 제한적이라는 것은 많은 바이러스 게놈이 1600개 이상의 DNA nucleotide를 추가로 삽입할 수 없음을 의미합니다. 바이러스는 34kDa 크기의 RLuc reporter에 대해 더 내성이 있지만, 생성되는 blue light가 동물 모델에서 쉽게 분산되므로 이미징에 어려움이 있습니다. NLuc의 blue light를 이용한 이미징은 동물 모델에서 측정이 어렵지만, 발광의 밝기와 긴 발광 signal을 비롯한 작은 크기로 인해 상당한 이점이 있습니다. Gaussia luciferase도 작고 밝은 luciferase이지만 세포 밖으로 배출되는 특징과 짧은 flash signal로 인해 in vivo에서의 작업이 어렵습니다.
여기에서는 NLuc의 크기를 이용하여 더 우수하고 안정적인 재조합 바이러스를 만든 두 가지 예시를 설명하고자 합니다. Peer-reviewed 논문에 인용된 NLuc이 포함한 바이러스 또는 virus-like particle 관련 추가적인 리스트는표 1을 참조하세요. 최근 도입된 11개의 아미노산으로 구성된 발광 단백질 tag은 구조적 보완(structural complementation)되어 functional luciferase를 만들 수 있으며 이는 바이러스 연구에도 적용될 수 있습니다. HiBiT라고 하는 이 작은 펩타이드 tag을 사용한 두 건의 초기 논문 내용은 NLuc full-length에 대한 섹션 이후에 이어집니다.

그림 1. Firefly (FLuc), Renilla (RLuc), NanoLuc® (NLuc) luciferase와 HiBiT 발광 단백질 (bioluminescent protein) tag의 코딩 영역(coding region) 크기 비교 각 luciferase의 크기는 그래프에서 각 막대의 오른쪽에 kDa 단위로 표시함
실험방법
원래의 바이러스와 거의 유사한, 복제 가능한 reporter 인플루엔자 A 바이러스의 생성
인플루엔자 reporter 바이러스의 생성이 어려운 이유는 여러 가지가 있습니다(3).
- 모든 바이러스 유전자는 in vivo에서 필수적이며, reporter로 간단한 유전자 대체를 불가능하게 합니다.
- 작은 게놈은 크기가 큰 유전자 삽입(insertion)을 용납하지 않으며, 이는 시간이 지나면서 불안정해지고 소실됩니다.
- 삽입은 복제를 심각하게 감쇠시킬 수 있습니다.
- 코딩 영역(coding region)의 끝부분에 삽입되면 패키징이 중단될 수 있습니다.
인플루엔자 reporter 바이러스는 세포 배양 모델이 아닌 살아있는 동물에서 감염 과정을 실시간으로 분석할 수 있습니다. 이는 신종 인플루엔자 바이러스의 병원성 및 전염 가능성을 확인하는데 있어 중요합니다.
Tran 등(4)은 재조합 바이러스 디자인에 작고 밝은 NLuc과 현명한 접근 방식을 사용하여 이러한 문제점들을 극복했습니다. 중합효소(polymerase)의 subunit PA 유전자는 C-말단에 삽입이 가능한 것으로 알려져 있어, integration site로 선택하였습니다. PA-NLuc fusion은 PA와 동일한 활성을 나타낼 것으로 예상되었지만, porcine teschovirus에서 유래된 자가 절단(self-cleaving) 2A 펩타이드를 linker (결과적으로 PA와 NLuc 단백질이 각각으로 만들어짐)로 사용하여 바이러스 construct를 만들어 trafficking과 assembly와 같은 PA의 다른 기능에 관련된 문제를 방지하였습니다.
재조합 NLuc 바이러스는 배양 및 in vivo에서 원래의 바이러스의 특성으로 복제되었습니다. 리바비린(ribavirin) 처리하여 NLuc 발광이 NLuc의 비특이적인 carryover나 패키징으로 인한 것이 아니라 유전자 발현으로 인한 것임을 입증하였습니다. 플라크 형성 단위와 발광을 비교한 세포 기반 assay에서 상관 관계가 높게 나타났으며 (r2 = 0.99), NLuc assay는 48~72시간 플라크 assay에 비해 8시간이 소요된다는 이점이 있습니다.
NLuc 바이러스는 마우스에서 모 바이러스와 구분되지 않는 병원성 및 치사력을 나타냈습니다. 이 바이러스는 in vivo 이미징을 수행하여 바이러스 부하(viral loads)과 마우스 폐로의 감염 확산을 추적하는데 사용되었습니다. 조류 인플루엔자 A 균주의 복제를 억제하는 것으로 알려진 돌연변이는 NLuc 바이러스와 동일한 표현형으로 생성되는 것을 확인하였습니다. 따라서 이 reporter 바이러스로 신종 바이러스를 평가할 수 있을 뿐 아니라 동물 모델에서 항바이러스제를 평가할 수 있습니다. 이후 진행된 연구에서는 페렛 모델에서 NLuc이 발현되는 H1N1 인플루엔자 A 바이러스의 접촉 및 공기 매개 전파도 입증하였습니다(4).
NanoLuc® Luciferase 삽입은 안정적이고 복제 가능한 reporter 알파 바이러스를 생성한다.
In vitro와 동물 모델에서의 바이러스 복제를 추적하기 위한 reporter 알파 바이러스(alphavirus)가 존재하지만, FLuc reporter 유전자의 삽입에는 다음과 같은 몇 가지 단점이 있습니다.
- 빠른 도입유전자(transgene)의 소실 가능성
- 복제 감쇠
Sun 등(5)은 다른 integration site을 선택하고 NLuc을 사용하여 이러한 문제를 해결하려 하였습니다.
이전 연구에서는 nonstructural protein 3 (nsP3)의 잘 보존되지 않은 C-terminal half에 직접 reporter를 fusion하였습니다. Sun 등은 FLuc (61kDa; 1,650 nucleotides) 또는 NLuc (19kDa; 513 nucleotides)을 사용하여 Sindbis, Chikungunya, Eastern and Venezuelan equine encephalitis virus의 해당 부위를 표적으로 삼았습니다. 다른 표적 부위와 전략도 조사하였습니다. 캡시드와 PE2 단백질 사이의 삽입 부위에는 단백질 fusion 없이 report를 생성하기 위해 Trosea asigna 바이러스 (TaV) 펩타이드 2A 서열과 함께 FLuc과 NLuc을 사용하였습니다. 또한 luciferase가 바이러스성 단백질과 fusion 되진 않지만 여전히 바이러스 게놈의 일부인 subgenomic promotor로부터 NLuc 또는 Fluc을 발현하는 재조합 바이러스가 생성되었습니다.
삽입 방법과 무관하게 FLuc이 포함된 삽입 유전자는 빠르게 손실되었으며 이는 세포 계대에 따른 발광 감소와 western blot을 통해 발현 단백질의 손실을 보여주었습니다. NLuc construct는 매우 안정적이었으며, FLuc 또는 NLuc과 fusion된 nsP3는 nsP3 유전자 단독에 비해 낮은 발현율이 관찰되었습니다. 치사성(lethality) 연구에서는 TaV-NLuc construct가 모 바이러스만큼 치명적임을 확인하였습니다. 동물 모델의 이미징에서 NLuc 발현 바이러스가 in vivo에서 복제되고 동물 전체에 퍼지는 반면, Fluc 발현 바이러스의 발광은 반복 복제 후 삽입된 Fluc 유전자가 소실되어 주사 부위에 국한됨을 확인하였습니다.
HiBiT 발광 단백질 tag을 이용한 연구
2016년 단백질 구조 보완 기술(structural complementation technology)의 NanoLuc Binary Technology (NanoBiT)이 도입되었습니다(6). 최초의 peer-reviewed 논문은 NLuc의 아미노산 156-157를 나누어 156개의 아미노산 subunit과 13개의 아미노산 subunit을 개발하는 방법에 초점을 맞추었습니다. 큰 subunit의 안정성과 발현을 개선하기 위해 engineering하여 LgBiT subunit을 만들었으며, 이 LgBiT은 효소 활성이 거의 없습니다. 350개 이상의 13개 아미노산 펩타이드를 합성하여 LgBiT에 대한 결합 특성과 LgBiT의 구조적 보완 (structural complementation)에 대해 테스트하여 새로운 기능적 효소인 NanoBiT® luciferase를 생성하였습니다. 그 중 두 가지 펩타이드가 두드러진 결과를 보였습니다. 하나는 LgBiT에 대한 낮은 affinity를 가지는 SmBiT이고 다른 하나는 LgBiT에 대한 높은 affinity를 갖는 HiBiT입니다. LgBiT과 SmBiT subunit은 관심 단백질의 affinity로 인해 LgBiT과 SmBiT이 결합할 수 있을 만큼 충분히 근접한 경우 NanoBiT luciferase가 생성되기 때문에 단백질-단백질 상호작용을 측정하는데 사용할 수 있습니다. 단백질-단백질 상호 작용에 대한 이러한 분자내 연구(intramolecular study)는 NanoBiT® Protein:Protein Interaction System을 사용하여 진행할 수 있습니다.
HiBiT은 자발적으로 LgBiT과 결합하여 NLuc과 비슷한 밝기의 NanoBIT® luciferase를 형성합니다. Schwinn 등에 의한 연구(7)에서는 발광 단백질 tag으로서 HiBiT subunit의 유용성을 조사하였습니다. HiBiT tag (11개의 아미노산)은 단백질에 붙일 수 있으며, 이 fusion은 LgBiT subunit과 furimazine 기질이 포함된 시약을 사용하여 측정할 수 있습니다. HiBiT tag 단백질은 Nano-Glo® HiBiT Lytic Detection System, Nano-Glo® HiBiT Extracellular Detection System, Nano-Glo® HiBiT Blotting System (HiBiT tag 단백질을 Western blot으로 확인하는 시약) 3가지 시약을 사용하여 측정할 수 있습니다.
NLuc의 작은 크기로 인해 바이러스 연구가 가속화된 것처럼 HiBiT의 효과도 유망해 보입니다. 이제는 NLuc과 같은 169개의 아미노산 (~500 nucleotides) reporter를 이용하지 않아도 작은 11개의 아미노산 (33 nucleotides)을 삽입하기만 하면 됩니다. HiBiT tag이 바이러스학에서 어떻게 사용될 수 있는지에 대한 초기 사례가 이미 발표되었습니다.
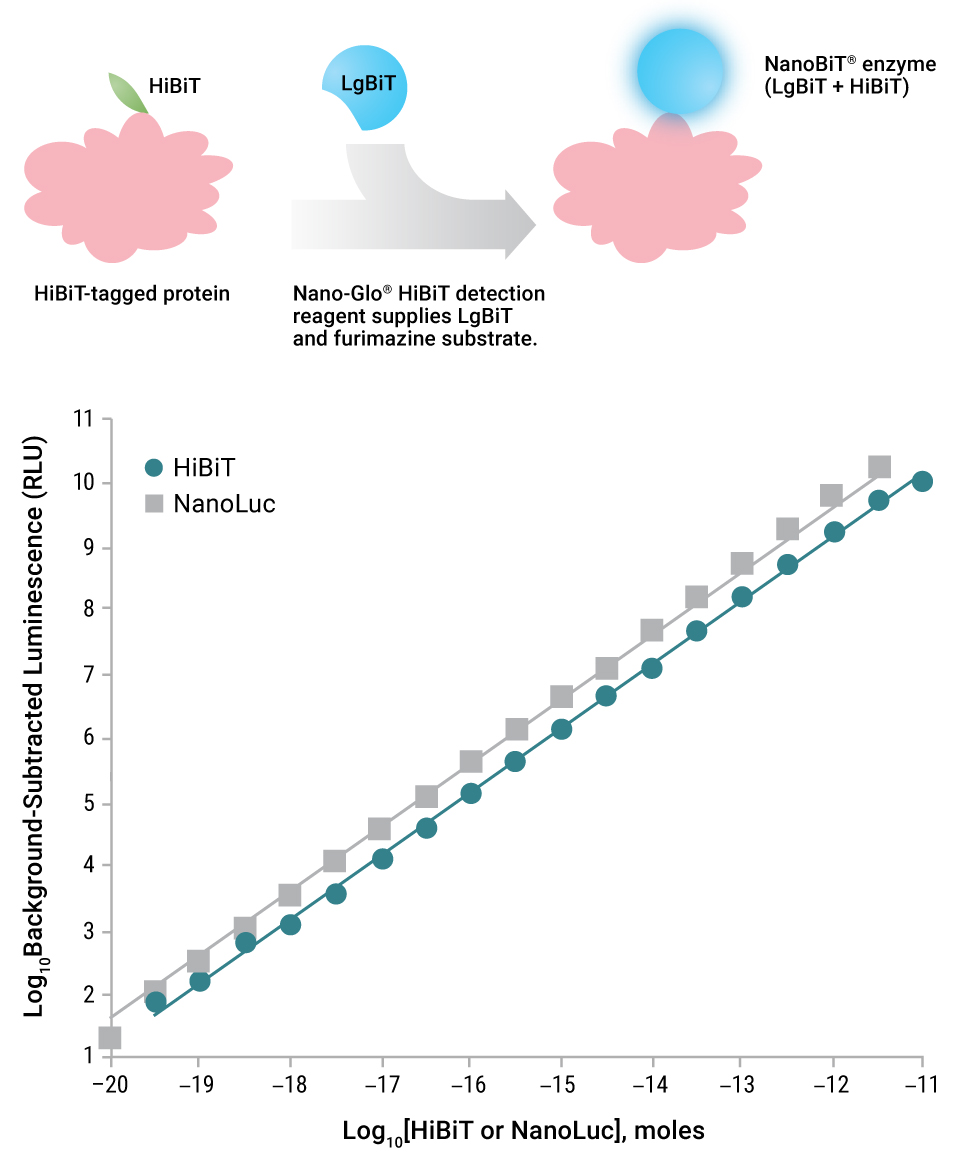
그림 2. Nano-Glo® Detection System을 이용한 HiBiT 검출 모식도(상단)과 HiBiT/LgBiT NanoBiT® luciferase에 의해 생성되는 발광 signal의 linearity(하단) Full-length재조합 NanoLuc® luciferase 또는 과량의 LgBiT과 HaloTag®-HiBiT 반응에 의해 생성된 발광 값을 그래프로 표시함
HiBiT tagging 은 West Nile 바이러스 침입과 방출에 대한 연구를 간소화한다.
West Nile 바이러스와 같은 플라비바이러스(flavivirus)는 일반적으로 기존의 바이러스 연구를 진행하기 위해 생물밀폐(biocontainment) 시설이 필요합니다. 표적 세포에 바이러스 부착과 바이러스 입자의 방출에 대한 연구에는 바이러스의 전체 게놈이 필요하지 않습니다. 단순히 구조 단백질이 포함된 plasmid를 숙주 세포에 넣어주면 소포체에서 바이러스 유사 입자(viral-like particle)가 출아(budding)하고 세포에서 분비됩니다. 이러한 subviral particle(SVP)은 생물밀폐 시설 없이도 바이러스의 세포 부착 관련 연구 시에 사용할 수 있습니다.
Sasaki 등(8)은 West Nile 바이러스의 entry 억제제를 찾는 시스템을 개발하였습니다. 이와 같은 실험은 바이러스 입자의 수를 정량화하기 위해 ELISA 기반 assay에 의존하였습니다. 최상의 조건에서 assay는 최소 2시간이 걸리고 정량 범위가 제한적 (~2배)입니다. HiBiT을 E 단백질의 내부 SVP 루프(intro-SVP loop)에 삽입하여 HiBiT-subviral particle(SVP-HiBiT)을 만드는데 사용하였습니다. 바이러스 M 단백질과 HiBiT-E 단백질이 포함된 plasmid를 293T 세포에 transfection하였고, 48시간 동안 배양한 배지 샘플에서 HiBiT-SVP 발현은 Nano-Glo® HiBiT Extracellular Detection System을 사용하여 모니터닝할 수 있습니다. Nano-Glo ® HiBiT Assay는 10분 만에 넓은 정량 범위 (~다섯 배)를 보여줍니다. HiBiT 염기서열의 존재는 Nano-Glo® HiBiT Blotting System을 사용한 Western blot으로 확인하였습니다. Rab11 G 단백질의 siRNA knockdown은 기존의 West Nile SVP의 분비를 크게 감소시키고 이와 마찬가지로 HiBiT-SVP의 분비를 억제하였습니다.
HiBiT technology는 바이러스와 subviral particle을 높은 감도로 검출할 수 있도록 합니다.
E와 M 단백질과 함께 West Nile 바이러스의 캡시드 단백질과 패키징 염기서열이 있는 subgenomic RNA를 만드는 construct를 포함하면 West Nile 바이러스 바이러스 유사 입자 (VLP)이 생성됩니다. 이러한 VLP는 발현을 위해 표적 세포에 유전자를 전달할 수 있습니다. 또한 VLP를 이용한 세포 부착을 측정할 수 있으며, subgenomic RNA는 바이러스 internalization을 보여주는 reporter를 포함할 수 있습니다. HiBiT 염기서열은 캡시드 단백질의 C-말단에 추가하고, LgBiT 단백질을 안정적으로 발현하는 Vero 세포주를 사용하여 VLP-HiBiT의 부착과 internalization를 모니터링하였습니다. VLP-HiBiT가 internalization 될 때 만들어지는 NanoBiT® luciferase는 Nano-Glo® Live Cell Assay System을 사용하여 모니터링하였습니다. NLuc-VLP는 바이러스 침입 억제제 (이 경우 West Nile 바이러스 E 단백질의 항체 또는 clathrin-coated pit 형성 억제제)를 스크리닝하는 방법을 보여주기 위해 사용되었습니다.
HiBiT기술은 다른 바이러스-세포 상호 작용 모델 시스템에 적용되었다.
Yamamoto 등(9)은 유사한 HiBiT 전략으로 CD4, CCR5 및 HaloTag®-LgBiT fusion이 발현하도록 제조된 HEK 293 세포주를 이용하여 HIV-1 VLP의 gp41-dependent cell fusion을 측정하였습니다. 이 assay는 세포 융합을 모니터링하고 gp41 염기서열의 site-directed mutagenesis를 허용하여 중요한 잔기를 식별할 수 있었습니다.
Torriani 등(10)은 endosome에서 아레나바이러스(arenavirus)-표적 세포 융합을 mimic하기 위한 세포 assay를 개발하였습니다. 아레나바이러스의 GP 단백질을 발현하는 두 개의 VeroE6 세포주를 만들었으며 각각의 세포에는 GFP와 LgBiT, RFP와 HiBiT를 발현시켰습니다. 두 세포를 혼합하고 세포 외부의 pH가 낮아지면 두 세포주의 융합이 일어나고 이 융합은 형광 이미지와 NanoBIT® luciferase 형성을 통해 확인하였습니다. 이러한 융합은 KCa3.1 calcium-activated potassium channel blocker인 TRAM-34에 의해 차단될 수 있습니다. TRAM-34 처리는 마츄포 바이러스(Machupo virus) 또는 림프구성 맥락수막염 바이러스(lymphocytic choriomening virus)의 GP 단백질에 의해 매개되는 융합을 차단할 수 있습니다.
HiBiT tagging은 native 바이러스와 유사하게 복제하는 더 우수한 reporter 플라비바이러스를 생성한다.
Reporter 바이러스는 바이러스 수명 주기를 확인하고 필요한 숙주 세포 단백질을 확인하는데 유용합니다. Puig-Basagoiti 등(11)은 재조합 NLuc-C형 간염 바이러스(HCV)를 이용하여 바이러스 분비에서 숙주 apolipoprotein E의 중요성을 확인하였습니다. 연구진은 full-length NLuc을 포함한 바이러스 복제의 차이에 대해 우려하였으며, 더 나은 복제 동역학(replication dynamics)을 가진 report 바이러스를 생산하기 위해 HiBiT tag을 테스트하였습니다(12). 연구진은 HiBiT tag이 붙은 HCV, 뎅기(DNV), 일본뇌염(JEV), 소바이러스성 설사(BVDV) 바이러스를 만들었으며, full-length reporter가 포함된 바이러스보다 높은 복제 능력으로 안정적인 HiBiT reporter 바이러스를 회수하였습니다.
LgBiT를 안정적으로 발현하는 세포에서 혹은 Nano-Glo® HiBiT Lytic Detection Reagent를 사용하여 재조합 바이러스 감염성과 복제율을 확인하기 위한 in vitro 실험을 수행하였습니다. HiBiT-HCV는 바이러스 분비에서 apolipoprotein E의 중요성을 확인하였습니다. HiBiT-JEV는 햄스터 (BHK21), 사람 (HeLa, A549, Huh7), 원숭이 (Vero E6) 및 모기 (C6/36)를 포함한 다양한 숙주 세포에서 복제되었습니다. HiBiT-DENV는 사람과 모기 세포에서만 테스트되었으며, 복제되는 것을 확인했습니다. BVDV를 사용하면, HiBiT는 바이러스의 외막 단백질과 fusion되었으며, 실험실에서는 HiBiT fusion이 바이러스 입자 형성을 변경할 것이라고 우려했습니다. 그러나 HiBiT fusion은 wide-type 바이러스와 비교하여 차이가 없는 것으로 관찰되었습니다.
4개의 HiBiT 바이러스 모두를 대상으로 알려진 플라비바이러스 억제제에 대한 감수성과 모 바이러스와의 유사 거동을 시험하였습니다. HiBiT-HCV와 HiBiT-JEV를 사용하여 69개의 protease 억제제 패널을 스크리닝하였으며, 바이러스 역가 대신 luciferase 발광 값을 사용하여 억제 화합물을 확인하였습니다. 이 스크리닝에서는 알려진 HCV 억제제를 확인하고, HiBiT-JEV에 효과적인 화합물을 밝혀 냈으며 HiBiT-DENV에 효과적임을 순차적으로 확인하였습니다. HiBiT-HCV는 인간 간 키메라 마우스 모델(human liver chimeric mouse model)에서 복제되었으며 HCV 억제제 치료에 반응하는 것으로 나타났습니다.
바이러스 단백질:숙주 단백질 상호작용 연구
NanoBiT® Protein:Protein Interaction Assays
앞서 언급한 바와 같이 NanoBiT® Protein:Protein Interaction (PPI) Assay는 친화성이 낮은 SmBiT과 LgBiT subunit으로 구성되어 있습니다(6). SmBiT과 LgBiT의 상호작용은 자발적으로 발생하지 않고 두 subunit이 상호 작용할 수 있도록 충분히 근접하게 하여 PPI를 연구하는데 이상적입니다. HiBiT-LgBiT과 같은 pair는 밝은 NanoBiT® luciferase를 형성합니다.
Sekiba 등(13, 14)은NanoBiT® Assay를 사용하여 B형 간염 바이러스 단백질인 HBx와 HEK 293와 HepG2 세포의 숙주 DDB1 단백질과 상호작용하는 억제제를 찾고자 했습니다. 이 assay를 사용하여 800개 이상의 FDA 승인 화합물을 스크리닝하였으며, 상호작용을 40% 이상 억제하는 5개의 화합물을 확인하였습니다. 가장 강력한 억제제인 니타옥사나이드(nitazoxanide)가 추가 연구를 위해 선택되었습니다.
Rawle 등(15)은 바이러스와 숙주 단백질을 모두 포함하는 HIV-1 reverse transcription complex의 억제제를 찾고자 하였습니다. Viral p66에 결합하지만 eEF1A에는 결합하지 않는 억제제를 사용하여 viral p66-host eEF1A 단백질의 상호작용을 저해하는데 중점을 두었습니다. NanoBIT® PPI Assay는 HEK 293T 세포에서 >70% 세포 생존율을 유지하면서 1,200개 이상의 scaffold를 스크리닝하여 40% 이상의 inhibition을 나타나는 물질을 찾는 실험을 디자인하였습니다. Rawle등은 추가 검사를 위해 후보 화합물 9개를 선정하였으며, 또한 Zika 바이러스의 NS2B와 NS3 단백질을 사용하여 양성 대조군인 NanoBIT® PPI pair를 구축하였습니다.
인간 헤르페스 바이러스 8(human herpes virus 8)로도 알려져 있는 Karposi’s sarcoma-associated herpesvirus (KSHV)는 사람의 여러 암과 관련되어 있으며, KSHV latency-associated nuclear antigen (LANA)은 KSHV의 잠재 기간에 감염의 확립에 중요합니다. LANA의 중요한 부분은 host SUMO2 interaction domain입니다. Ding 등(16)은 약초를 기반으로 한 천연물질 라이브러리에서 LANA-SUMO2 상호작용을 저해하는 small molecule을 찾아냈습니다. NanoBIT® Assay는 HEK 293 세포에서 디자인되었으며, 이 스크리닝을 통해 열대성 상록수에서 강력하고 효과적인 억제제를 찾아냈습니다. 이 억제제는 세포 모델에서 1차 감염과 잠복기(latency) 동안의 감염을 차단하였습니다.
NanoBRET® Protein:Protein Interaction Assays
Bioluminescent resonance energy transfer (BRET)은 단백질:단백질 상호작용을 모니터링하기 위해 일반적으로 사용되는 기술입니다. BRET을 사용하면 한 쌍의 단백질이 서로 근접하면 (10nm 미만) luciferase에서 만들어진 빛이 형광 수용체(fluorescent acceptor)로 전달됩니다. 대부분의 BRET 시스템은 RLuc 기반의 donor와 형광 단백질을 acceptor로 사용하지만, NanoBRET™ Assay(17)는 밝은 NLuc을 donor로, HaloTag® 단백질과 여기에 공유 결합하는 형광 dye를 acceptor로 사용합니다.
Nishi 등(18)은 B형 간염hepatitis B virus core protein (HBc)과 숙주 Pin1 단백질의 상호작용이 바이러스의 발병 기전에서 중요하다는 점을 발견하였습니다. 상호작용이 일어나기 위해서는 HBc 인산화가 필요합니다. 이 상호작용을 저해하는 phosphatase가 존재하는지를 확인하기 위해 연구진은 HEK 293 세포에 NanoBRET™ Assay를 사용하여 HaloTag® (HT) 단백질을 tagging한 150개의 phosphatase를 대상으로 NLuc-HBc과의 상호작용을 조사하였습니다. 이 스크리닝을 통해 두 개의 candidate이 확인되었으며, 하나는 pyruvate dehydrogenase phosphatase의 catalytic subunit으로 실제로 HBc를 dephosphorylation할 수 있었습니다.
Miyakawa 등(19)은 HIV-2 Viral Protein X (Vpx)와 숙주 단백질 SMHD1의 상호 작용으로 인해 분열하지 않는 세포에서 HIV-2 감염이 진행될 수 있다고 언급했습니다. SMHD1은 모든 세포의 dNTP를 가수 분해하여 분열되지 않은 세포에서 복제를 어렵게 만들 수 있습니다. Vpx와 SMHD1 상호작용은 ubiquitin ligase에 의한 polyubiquitination와 proteasome degradation을 통한 SMHD1 분해로 이어집니다. Vpx는 잘 알려진 인단백질(phosphoprotein)으로연구진은 SMHD1 상호작용에 Vpx phosphorylation이 필요함을 발견하였습니다. 412개 kinase에 대한 in vitro연구를 통해 50개의 kinase candidate를 확인하였습니다. 이는 NLuc-Vpx와 각각의 HT-kinase를 사용하여 HEK 293 세포에서 상호작용을 테스트하였습니다. 세 개의 kinase는 강한 NanoBRET™ signal를 보였으며 이 중 두 종류는 PIM kinase family의 kinase입니다. 추가 연구는 PIM 1, 2, 3에 대해 진행되었으며 흥미롭게도 NanoBRET™ Assay을 통해 PIM 인산화를 위한 serine이 없는 mutant Vpx는 SMHD1과의 상호작용을 심각하게 저해하였으나 ubiquitin ligase component와의 상호작용은 유지됨을 확인하였습니다.
NLuc는 작고 밝은 luciferase로서 여러 관심 바이러스의 게놈 크기에 최소한의 영향을 미치는 중요한 바이러스 연구 도구이다
결론
바이러스 연구는 바이러스성 질환이 어떻게 감염을 일으키고 전파되는지 이해하기 위해 필수적입니다. 재조합 reporter 바이러스는 연구자들이 바이러스의 내부 작용을 밝혀내는데 도움이 될 수 있습니다. 그러나 바이러스는 감염, 복제 및 전파를 위해 최소한의 게놈으로 진화하였으며, 자연 선택에 따른 생존에 부적합한 유전자(genomic baggage)를 잘 받아들이지 못합니다. NLuc은 작고 밝은 luciferase로서 여러 관심 바이러스의 게놈 크기에 최소한의 영향을 미치는 중요한 연구 도구입니다. HiBiT 발광 단백질 tag은 재조합 reporter 바이러스에 의해 운반될 때의 부담을 더욱 감소시켰으며 LgBiT과 결합하여 NLuc과 유사한 발광 signal를 생성합니다. NanoBiT® PPI Assay 와 NanoBRET™ Assay는 단백질 수준에서의 바이러스:숙주 상호작용을 연구할 수 있는 수단을 제공하였으며 상호 작용의 inhibitor와 상호 작용에 영향을 줄 수 있는 다른 숙주 단백질을 스크리닝하는데 사용되고 있습니다.
표 1. NanoLuc® luciferase를 이용한 만들어진 재조합 바이러스 또는 바이러스 유사 입자(Virus-Like Particles)
참고문헌
- Hall, M.P. et al. (2012) Engineered luciferase reporter from a deep sea shrimp utilizing a novel imidazopyrazinone substrate. ACS Chem. Biol. 7, 1848–57.
- Mehle, A. (2015) Fiat Luc: Biolumiescence imaging reveals in vivo viral replication dynamics. PLoS Pathog. 11, e1005081. PMID: 26356297.
- Tran, V. et al. (2013) Highly sensitive real-time in vivo imaging of an influenza reporter virus reveals dynamics of replication and spread. J. Virol. 87, 13321–9.
-
Karlsson, E.A., et al. (2015) Visualizing real-time influenza virus infection, transmission and protection in ferrets. Nat. Comm. 6, 6378. PMID: 25744559
- Sun, C. et al. (2014) Stable, high-level expression of reporter proteins from improved alphavirus expression vectors to track replication and dissemination during encephalitic and arthritogenic disease. J. Virol. 88, 2035–46.
- Dixon, A.S. et al. (2016) NanoLuc complementation reporter optimized for accurate measurement of protein interactions in cells. ACS Chem. Biol. 11, 400–8.
- Schwinn, M. et al. (2018) CRISPR-mediated tagging of endogenous proteins with a luminescent peptide. ACS Chem. Biol. 13, 467–74.
- Sasaki, M. et al. (2018) Development of a rapid and quantitative method for the analysis of viral entry and release using a NanoLuc luciferase complementation assay. Virus Res. 243, 69–74.
- Yamamoto, M., et al. (2019) Cell-cell fusion and virus-cell fusion assay-based analyses of alanine insertion mutants in the distal α9 portion of JRFL gp41 subunit from HIV-1. J. Biol. Chem. 294, 5677-87.
- Torriani, G., et al. (2019) Identification of clorimazole derivatives as specific inhibitors of arenavirus fusion. J. Virol. 93, e01744-18.
- Puig-Basagoiti, F. et al. (2016) Human cathelicidin compensates for the role of apolipoproteins in hepatitis C virus infectious particle formation. J. Virol. 90, 8464–77.
- Tamura, T. et al. (2018) Characterization of recombinant Flaviviridae viruses possessing a small reporter tag.J. Virol. 92, e01582–17.
- Sekiba, K., et al. (2019) Inhibition of HBV transcription from cccDNA with nitazoxanide by targeting the HBx-DDB1 interaction. Cell. Mol. Gastroenterol. Hepatol. 7, 297-312.
- Sekiba, K., Otsuka, M.,and Koike, K. (2019) Identifying inhibitors of the HBx-DDB1 interaction using a split luciferase assay system. J. Vis. Exp. 154, e60652.
- Rawle, D.J., et al. (2019) Oxazole-benzenesulfonamide derivatives inhibit HIV-1 reverse transcriptase interaction with cellular eEF1A and reduce viral replication. J. Virol. 93, e00239-19.
- Ding, L., et al. (2019) Identification of viral SIM-SUMO2-interaction inhibitors for treating primary effusion lymphoma. PLoS Pathog. 15, e1008174.
- Machleidt, T., et al. (2015) NanoBRET-A novel BRET platform for the analysis of protein-protein interactions. ACS Chem. Biol. 10, 1797-804.
- Nishi, M., et al. (2020) Prolyl isomerase Pin1 regulates the stability of hepatitis B virus core protein. Front. Cell Dev. Biol. 8, 26.
- Miyakawa, K., et al. (2019) PIM kinases facilitate lentiviral evasion from SAMHD1 restriction via Vpx phosphorylation. Nat. Comm. 10, 1844.
Related Products
NanoBiT® PPI Starter Systems
Detects interactions at low expression levels and allows real-time kinetic analysis in live cells
NanoBiT PPI systems are based on reversible protein complementation reporter technology. These systems can be used to detect interactions at low expression levels and allow real-time kinetic analysis in live cells.
HiBiT Protein Tagging System
HiBiT simplifies protein detection, providing a streamlined, antibody-free protocol for detecting tagged proteins using a convenient, bioluminescence based method.
NanoBRET® PPI Starter Systems
BRET-based technology to detect protein interactions in real time using full-length proteins or fragments. The reversible assay technology allows you to study both induction and inhibition of protein interactions. Assays can be performed in 96- or 384-well formats.
NanoGlo® Luciferase Assay Systems
The NanoGlo® Luciferase Assay System is a single-addition reagent that generates a glow-type signal in the presence of NanoLuc® luciferase with a half-life of approximately 120 minutes in commonly used tissue culture media. The Nano-Glo® Live Cell Assay System is used to measure NanoBiT® or NanoLuc® luminescence from living cells.