단백질 Tagging: 단백질 Tag 선택 방법
Sara Klink
Promega Corporation
게시일: 7/2019
초록
단백질 tagging은 단백질 분석에서 중요한 부분입니다. 단백질 분리, 정제, pull-down assay, immunoassay 등의 다양한 응용 분야에서 단백질 tagging이 사용되고 있으며 여러분의 단백질 기능 확인 연구에 도움을 주고 있습니다. 그렇다면 어떤 단백질 tag를 선택해야 할까요? 이 article에서는 실험에 도움이 되는affinity 기반의 tag (affinity-based tag) 또는 reporter 기반의 tag (reporter-based tag)과 시약에 대해 이야기하고자 합니다.
서론
단백질이나 peptide는 세포 기능에 있어 필수적이며 에너지 대사, 세포 성장, 신호 전달, 분열 주기 및 세포사멸과 관련한 pathway를 구성하는 효소입니다. 특정 단백질을 분리하고 검출한다는 것은 어떤 단백질이 더 큰 단백질 complex의 일부인지, 어떤 단백질과 상호 작용하는지, 세포 기능과 질병에서 어떤 역할을 하는지 등을 이해할 수 있게 합니다. 이러한 단백질의 기능을 연구하는 방법 중 하나는 타겟 단백질에 tag을 추가하여 cell lysate로부터 해당 단백질을 분리한 후 이를 연구하는 것입니다.
Fusion tag는 peptide, 작은 크기의 단백질 또는 효소 단백질의 아미노 (N) 또는 카르복실 (C) 말단에 붙일 수 있습니다. Vector cloning을 통해 tagging하거나 CRISPR-Cas9 유전자 편집(gene editing)을 사용하여 endogenous 단백질에 tag를 추가할 수 있습니다. Affinity tag을 사용하여 단백질을 분리하거나 고정시켜 proteomics 연구를 추가적으로 수행할 수 있습니다.
일반적으로 연구자들은 단백질 tagging을 통해cell lysate에서 단백질을 정제하고 이를 biochemical assay에 사용하지만, peptide tag를 사용하게 되면 더 많은 연구에 활용할 수 있습니다. 예를 들어, 단백질에 특이적으로 결합하는 항체가 없는 경우 tag 특이적인 항체(tag-specific antibody)를 사용하여 tagging 단백질을 검출할 수 있습니다. 또한 tag으로 단백질을 정량하고, 단백질 complex를 연구할 수 있으며, 단백질이 세포 내부 또는 외부에 있는지 확인할 수 있습니다. 또한, 단백질 tag을 사용하여 세포 내의 단백질 위치도 시각화할 수 있습니다.
그렇다면 어떤 단백질 tag이 실험에 적합할까요? 아래는 단백질 tagging을 위한 유용한 tool 목록입니다.
Polyhistidine
구조가 가장 간단하고 가장 작은 tag 중 하나는 polyhistidine tag 또는 6xHis tag입니다. 일반적으로 이 peptide tag은 단백질 N 또는 C 말단에 붙일 수 있는 히스티딘(histidine) 아미노산 6개로 구성됩니다. His tag은 크기가 작아 단백질의 구조를 변형시키지 않는 특징이 있어 downstream assay에 유용합니다. 또한, His tag은 Ni2+, Zn2+, Cu2+와 같은 금속 이온에 결합할 수 있어 fusion 단백질을 정제하거나 고정시키는데 유용합니다.
Polyhistidine tag은 E. coli에서 발현되는 단백질을 빠르게 정제하는 데 유용하지만 포유류 또는 곤충 세포에서 발현되는 단백질의 경우 히스티딘 잔기의 수가 많을수록 더 높은 background binding을 보여집니다. 따라서 단백질 순도를 높이려면 His-tagged protein이 결합된 metal resin을 잘 washing 해 주어야 합니다. 또한 8M urea나 6M guanidine HCl과 같은 denaturing agent를 His-tagged membrane 또는 insoluble protein과 함께 사용하면 정제 과정을 개선할 수 있습니다.
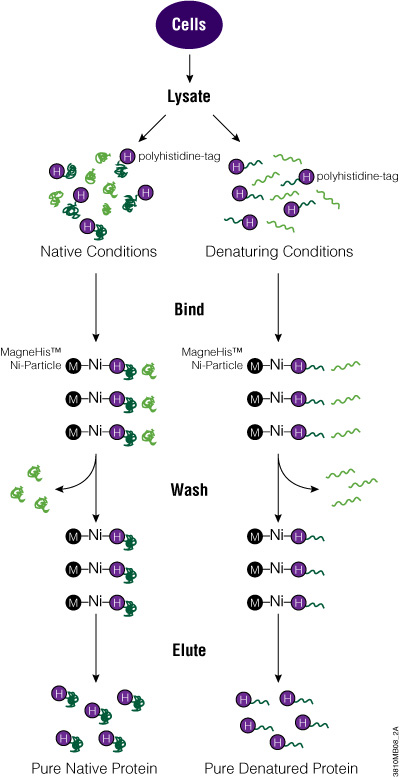
His tag를 단백질에 tagging하려면 tag이 포함된 vector에 타겟 단백질의 ORF를 cloning해야 합니다. 사용된 promoter에 따라 박테리아, 포유류 또는 곤충 세포에서 tagging 단백질을 발현시킬 수 있습니다. 다른 방법으로 cell-free expression 시스템을 사용하여 단백질을 발현시킬 수 있습니다. 단백질을 정제하기 위해 cell lysate에 magnetic bead (예: MagneHis™ Protein Purification System) 또는 non-magnetic resin (예: HisLink™ Protein Purification System)를 사용할 수 있습니다. 만약 His-tagged 단백질을 Rabbit reticulocyte lysate-based system에서 발현시켰다면 MagZ™ Protein Purification System을 사용하면 헤모글로빈을 최소화한 단백질 정제가 가능합니다. Purification 매트릭스에서 tagging 단백질을 elution한 후 이 단백질은 바로 다음 연구에 사용할 수 있습니다.
Polyhistidine-Tagged Protein 정제
Glutathione-S-Transferase (GST)
GST (Glutathione-S-Transferase)는 bacterial lysate에서 tagging 단백질을 정제하기 위해 E. coli에서 발현되는 단백질에 사용되는 affinity tag입니다. 이 26kDa의 peptide tag은 진핵세포에 존재하는 세포질 단백질 계열의 일부이므로, 진핵세포에서 타겟 단백질을 분리할 때 다른 단백질과 경쟁하기 때문에 그 유용성이 떨어집니다. 진핵생물의 단백질에 GST를 tagging하면 박테리아에서 발현되는 fusion 단백질의 용해도가 향상됩니다. 또한 GST-tagged 단백질은 박테리아에서 발현율이 높을 수 있지만 protein aggregation으로 인한inclusion body를 형성할 수 있습니다. GST tag는 타겟 단백질의 N 또는 C 말단에 추가할 수 있습니다.
GST는 glutathione에 대한 강한 affinity를 가집니다. 이는 glutathione-coated beads와 같은 고정화된 매트릭스에서 GST fusion 단백질을 capture할 수 있음을 의미합니다. 이 결합 특성은 단백질 정제뿐만 아니라 해당 단백질과 결합하는 단백질 (예: pull-down assay)을 capture하는 데 사용할 수 있습니다.
GST tagging 단백질은 발현율과 용해도가 높지만, tag 크기가 커서 downstream application에서 단백질 기능을 방해할 수 있습니다. GST fusion 단백질에서 GST tag을 잘라 기능적인 간섭을 줄일 수 있습니다. 발현된 단백질이 inclusion body로 응집된 경우 glutathione을 사용한 affinity purification는 불가능합니다. GST가 glutathione에 성공적으로 결합하려면 적절하게 folding되어 있어야 하며, GST tag가 refolding 되더라도 결합되지 않을 수 있습니다.
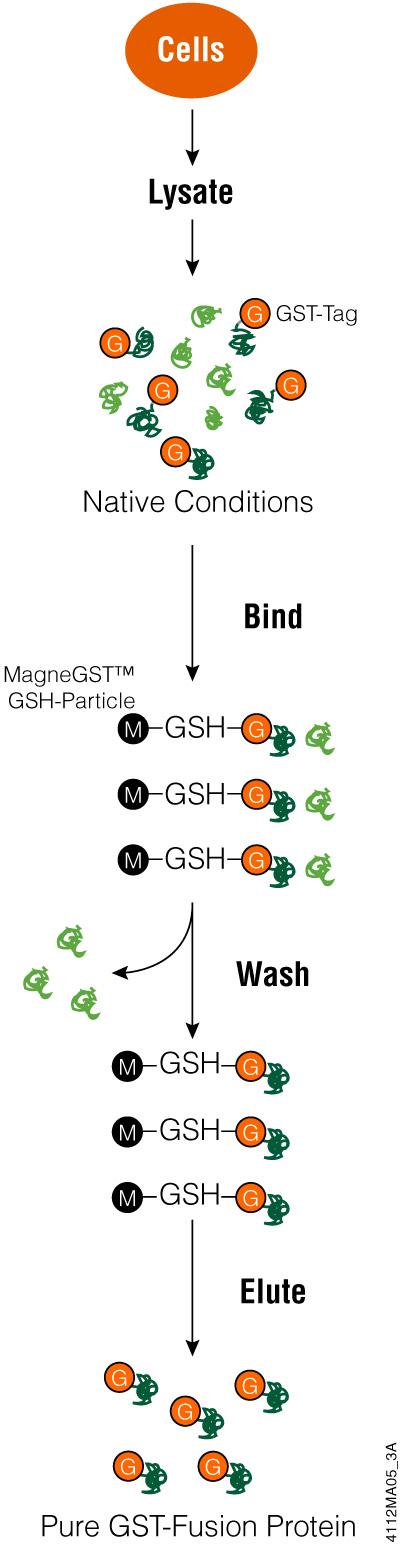
GST를 tagging 하려면 먼저 타겟 단백질의 coding region을 vector에 cloning하고 E coli에서 tagging 단백질을 발현시켜야 합니다. Inducible promoter를 사용하여 타겟 단백질의 발현을 조절하면 박테리아 세포에 독성을 가지는 단백질을 정제하는 데 도움이 될 수 있습니다. 박테리아 세포가 lysis되면 (예: FastBreak™ Cell Lysis Reagent)) glutathione-based resin (예: MagneGST™ Protein Purification System)을 사용하여 GST tag 단백질을 정제할 수 있습니다. 사용하는 cloning vector에 따라, 단백질에서 GST tag를 제거할 수 있는 protease 절단 부위가 존재할 수 있습니다. 단백질이 분리되거나 절단되면 분석 준비가 완료된 것입니다.
GST-fusion protein 정제하기
HaloTag® 단백질
GST tag와 6XHis tag는 박테리아 세포에서 발현되는 단백질을 분리하는 데 유용하지만 E. coli 및 포유류 세포에서도 모두 사용할 수 있는 tagging 옵션도 있습니다. 34kDa 크기의 HaloTag® 단백질은 species에 따른 발현 시스템에 유연성을 제공합니다. Non-covalent interaction을 사용하여 단백질을 정제하는 다른 tag와 달리 HaloTag® 기술의 핵심은 HaloTag® 단백질과 HaloTag® ligand와의 공유 결합(covalent bond)입니다. 공유 결합력 때문에, 엄격한 조건에서 tagging 단백질을 washing 할 수 있고 비특이적 단백질을 제거할 수 있습니다. Tag의 크기가 단백질의 기능에 미치는 영향에 대해 걱정하고 계신가요? 걱정하지 마세요! TEV protease를 사용하여 HaloTag에서 단백질을 잘라 분리하면, tagging되지 않은 단백질을 바로 다음 분석에 사용할 수 있습니다.
박테리아 세포에서의 단백질 발현에 있어 어려운 문제 중 하나는 용해도(solubility)입니다. 진핵생물의 단백질은 methylation되지 않고 E. coli에서 합성될 때 post-translational modification이 일어나지 않아 inclusion body를 형성하는 경향이 있습니다. HaloTag® 단백질과 같은 fusion tag은 재조합 단백질의 용해도를 높이고 박테리아에서의 발현을 향상시켜 원하는 단백질을 보다 쉽게 정제할 수 있습니다. 포유류 세포에서 HaloTag-fusion protein을 발현시키면 post-translational modification이 되며 이런 단백질은 세포 내에서의 기능을 더 유사하게 반영할 수 있습니다. HaloTag® ligand로 코팅된 resin과 같은 고정화된 매트릭스를 사용하면 HaloTag fusion 단백질만을 정제하거나, 타겟 단백질에 결합하는 단백질을 확인하기 위한 pull-down assay에도 사용할 수 있습니다. 이러한 방식으로, 단백질 간의 interaction을 더 잘 이해할 수 있습니다.
그러나 HaloTag®을 이용한 응용은 protein-protein interaction (PPI)과 단백질 정제로 끝나지 않습니다. 단백질에 결합하는 DNA 염기서열을 연구하는 경우, HaloTag® 기술을 사용하여 protein-DNA interaction을 해석할 수 있습니다. Immunochemistry에 무엇을 사용해야 할까요? 프로메가는 여기에 딱 맞는 항체를 제공합니다. 세포 이미징(cell imaging)에 관심이 있으십니까? 타겟 단백질에 HaloTag® 단백질을 fusion한 단백질과 형광 HaloTag® ligand를 사용하면 해당 단백질이 어디에 위치해 있는지, 단백질이 수송(trafficking)되는지, 얼마나 빨리 turnover되는지 확인할 수 있습니다. 초고분해능 현미경(super resolution microscopy)과 FACS용 ligand도 있습니다. HaloTag® 기술에 대한 자세한 내용은 여기에서 알아보세요.
HaloTag® 기술을 시작하려면, 기존의 cloning vector나 Flexi® cloning vector에 관심 단백질의 coding region을 cloning하여 N 또는 C 말단에 HaloTag를 넣어주세요. 또는 Kazusa에서 사전 제작된 수천 개의 HaloTag® clone을 검색 하여 이용할 수 있습니다. 한 번 clone을 만들어 놓으면, 모든 단백질 분석 응용 분야에 이를 사용할 수 있습니다. 다음에 수행하려는 실험에 따라 정제 시스템 (예: HaloTag® Mammalian Protein Purification System 또는 HaloTag® Protein Purification System)이나 pull-down assay (예: HaloTag® Mammalian Pull-Down Systems)가 필요할 수 있습니다. 이미징 연구의 경우, 올바른 fluorescent ligand (예: HaloTag® Ligands 또는 Janelia Fluor® HaloTag® Ligands)를 선택해야 합니다. 면역학 연구에 관심이 있으시다면, Anti-HaloTag® pAb가 도움이 될 것입니다. Protein interaction의 경우, protein-protein interaction 연구를 위한 NanoBRET™ PPI Systems과 단백질-DNA interaction 연구를 위한 HaloCHIP™ System이 있습니다.
HaloTag® Interchangeable Labeling Technology

앞에서 설명한 peptide tag의 대부분은 단백질 정제, pull-down assay 또는 tagging 단백질을 고체 매트릭스에 결합하는 방법에 사용되는 affinity tag이지만 다른 유형의 tag도 있습니다. 단백질 정량에서 endogenous tagging에 이르기까지 단백질에 fusion된 발광tag 또는 작은 크기의 reporter 단백질을 사용하여 세포에서 tagging 단백질을 추적할 수 있기 때문에 항체가 필요하지 않습니다.
HiBiT Peptide Tag
크기가 작은 tag은 여러 용도로 사용할 수 있으며 특히 11개의 아미노산의 펩타이드 tag인 HiBiT은 단백질 tagging에 적합합니다. 기존의 cloning 방식이 아닌 CRISPR 유전자 편집 방식을 통해 endogenous 단백질에 HiBiT tag를 추가할 수도 있습니다. 전통적인 plasmid를 이용한 exogenous 발현 시에 일반적으로 나타나는 과발현 없이 단백질을 연구할 수 있다는 장점이 있습니다. 타겟 단백질이 일반적으로 세포에서 발견되는 것과 동일한 비율로 유지되기 때문에, 생리학적 조건 하에서 tagging 단백질의 변화를 연구할 수 있습니다. 이는 단백질 과발현으로 인한 artifact가 적고 생물학적으로 관련성이 높은 결과를 얻을 수 있다는 것을 의미합니다. CRISPR를 사용하여 peptide tag를 추가하는 프로토콜은 간단하고, HiBiT의 작은 크기가 높은 편집 효율을 제공합니다.
HiBiT은 자체로는 발광되지 않습니다. 그러나 HiBiT에 보완적인 LgBiT 단백질이 포함된 검출 시약이 추가되면 밝은 발광signal이 생성됩니다. 이런 정량 가능한 값은 발광측정기(luminometer)를 사용하여 쉽게 측정할 수 있습니다. 발광 기법의 분석 방법은 감도가 높으며 nano mol 수준까지 검출이 가능합니다. 세포 밖의 단백질이나 분비된 단백질을 연구하고 싶으신가요? 여기에 딱 맞는 시약 시스템이 있습니다! HiBiT tagging 단백질을 정량할 때 Lytic system을 이용하고, 분비된 단백질을 측정할 때는 Extracellular system을 사용하세요. 항체 대신 프로메가의 Bioluminescent Blotting System을 사용하여 membrane에 blotting된 단백질을 검출할 수 있습니다. LgBiT을 세포 내에서 발현시킨 경우, 살아있는 세포에서 HiBiT-tagged 단백질의 양을 실시간으로 측정할 수 있습니다. 단백질 tagging으로 HiBiT을 사용하는 자세한 방법은 여기에서 확인하세요.
HiBiT를 사용하기 위한 첫 단계로 ORF를 기존의 MCS vector 또는 Flexi® vector 중 하나로 cloning하거나 CRISPR 방법을 사용하여 genome sequence에 HiBiT tag을 추가할 수 있습니다. 최적의 단백질 검출을 위해 tag을 적절한 위치에 넣어주세요. 먼저 HiBiT을 단백질에 tagging한 후, 연구에 가장 적합한 방법 (Nano-Glo® HiBiT Lytic, Intracellular 또는 Blotting Systems)을 선택하세요.
Overview of the Nano-Glo® HiBiT Lytic Detection System

HiBiT also makes an excellent epitope tag for those who would like to pursue more traditional immunological assays, expanding the protein analysis options beyond bioluminescent assays. For endogenous HiBiT-tagged proteins, the Anti-HiBiT Monoclonal Antibody (mAb) can confirm subcellular localization. Perform Western blotting to assess protein levels and size for proteins tagged with HiBiT. Immunoprecipitate HiBiT-tagged proteins to enrich for protein of interest or determine binding partners. You can even use the HiBiT tag and antibody for fluorescence-activated cell sorting (FACS) analysis on live or fixed cells. With subpicogram sensitivity and high specificity, the Anti-HiBiT mAb performs as well or better as other commonly used epitope tag antibodies, adding to the versatility of the HiBiT tag.
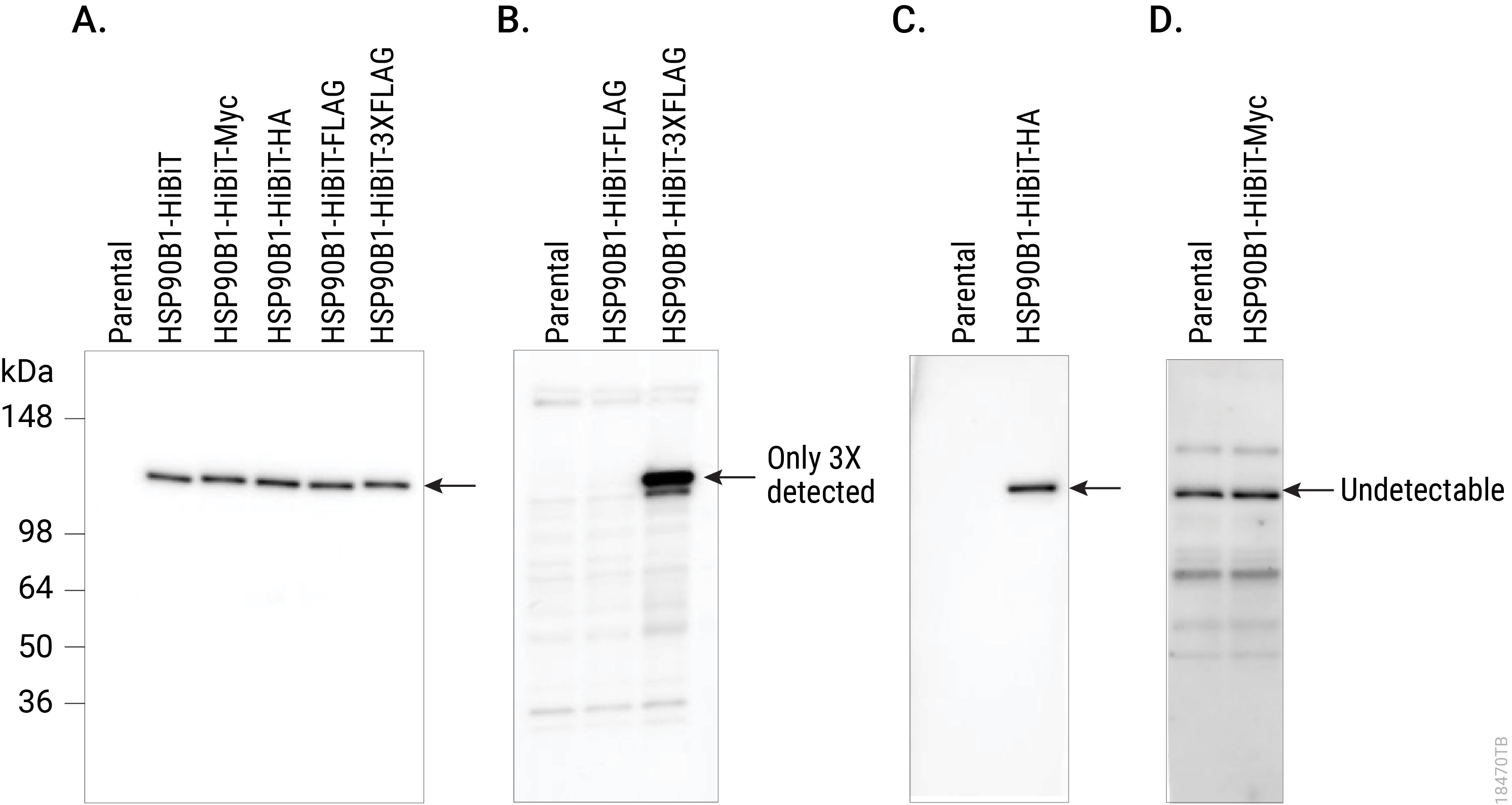
Comparing Western blot detection using Anti-HiBiT Monoclonal Antibody to common epitope tag antibodies. HSP90B1 was endogenously tagged on the C terminus in HeLa cells with HiBiT alone or HiBiT and a single copy of the Myc, HA or FLAG® tags, or three copies of the FLAG® tag. Lysates (10µg) from the HSP90B1-tagged cell pools were separated by SDS-PAGE. After transfer to PVDF membrane, Western blotting was performed with 1µg/ml Anti-HiBiT Monoclonal Antibody (Panel A), 10µg/ml Anti-FLAG® (M2; Panel B), 0.1µg/ml Anti-HA (3F10; Panel C) or 1µg/ml Anti-Myc (9E10; Panel D) primary antibodies and 0.4µg/ml anti-mouse or anti-rat (for anti-HA blot) secondary antibody and ECL substrate using a 5-minute exposure. The HiBiT antibody image brightness was scaled 0–29,817 and all other images 145–2,735.
To start using HiBiT, you can clone your ORF into one of our traditional MCS or Flexi® vectors or use a CRISPR method to add the tag to the genomic sequence. Place the tag where needed for optimal detection. Once your protein is tagged with HiBiT, determine which method works best for your studies (Nano-Glo® HiBiT Lytic, Extracellular or Blotting Systems). Alternatively, detect HiBiT using a sensitive antibody-based method with the Anti-HiBiT Monoclonal Antibody.
NanoLuc® Luciferase
가끔 reporter를 사용해야만 하는 경우가 있습니다. 다행히 NanoLuc® luciferase는 19kDa 효소로, 정상적인 세포 기능을 방해하지 않고 다른 단백질과 함께 수송될 수 있을 정도로 작은 크기의 발광 단백질입니다. HiBiT과 마찬가지로 NanoLuc은 감도가 높고 쉽게 정량화 할 수 있는 단백질 fusion tag입니다. 그러나 reporter enzyme은 보완적인 파트너가 필요하지 않아 일부 응용 분야에서 사용이 간편합니다. NanoLuc® luciferase는 크기가 작고 밝기 때문에 바이러스 입자에 어렵지 않게 도입할 수 있습니다. 바이러스학 연구자들이 어떻게 NanoLuc® luciferase을 바이러스 입자에 적용했는지에 관해 읽어보세요. Reporter enzyme인 NanoLuc® luciferase는 fusion 단백질의 세포 내 위치를 감지하고 단백질의 잠재적 pathway를 추적하는 데 도움이 됩니다. 또한 NanoLuc® fusion 단백질은 protein-protein interaction 또는 small molecule의 target engagement를 연구하기 위한 BRET (Bioluminescence Resonance Energy Transfer) 기법의 응용 분야에 사용할 수 있습니다. 이 reporter enzyme의 기능에 대해 자세히 알아보세요.
NanoLuc® luciferase와 단백질 fusion을 생성하려면 ORF를 NanoLuc® reporter vector에 cloning하여 NanoLuc를 N 또는 C 말단에 배치해야 합니다. 응용 분야에 따라 lytic detection system (예: Nano-Glo® Luciferase Assay System) 또는 live-cell detection assay (예: Nano-Glo® Live Cell Assay System)를 활용할 수 있습니다.
요약
단백질 tag의 선택은 진행하고자 하는 실험에 따라 달라집니다. 단백질 정제를 위한 affinity tag이 필요한지, 다양한 단백질 분석을 위한 single fusion protein을 생성해야 하는지, CRISPR/Cas9 유전자 편집을 사용하여 endogenous 단백질에 tag를 추가하고자 하는지에 따라 다양한 tag 및 reporter enzyme을 활용할 수 있습니다.