면역원성 세포사(Immunogenic Cell Death): DAMPs(Damage Associated Molecular Patterns)를 측정하는 방법
작성자: Andrew Niles, Kevin Kupcho
초록
지난 50년 동안 세포 사멸(cell death)에 대한 연구는 여러 가지 흥미로운 변화를 가져왔습니다. 현재 세포 사멸 메커니즘이 생명체에 전반적으로 주요한 영향을 미친다는 것은 보편적으로 받아들여지고 있으며 최근에는 immunogenic cell death (ICD)가 선천성 및 후천성 면역 반응에 미치는 영향에 대해 보고되고 있습니다. DAMPs (Damage Associated Molecular Patterns)는 ICD 과정 중에 생성되는 특이적 생체분자 메신저로, 이 과정의 진행과 규모를 조절합니다. 따라서 DAMPs의 존재를 사전에 조절하는 것은 건강과 질병에 중요한 영향을 미칩니다.
DAMPs 정량을 위한 기존의 분석 방법은 타당한 정보적 가치를 제공하지만 이를 구현하기 위해서는 많은 노력과 시간이 필요할 수 있습니다. 여기에서는 homogenous하고 일반 발광 기법을 사용하여 측정할 수 있는 두 가지의 새로운 발광 기법의 assay (RealTime-Glo™ Extracellular ATP Assay & Lumit™ HMGB1 Immunoassay)에 대해 설명하고자 합니다. 또한, 신뢰할 수 있고 강력한 이 두 가지 assay는 in vitro immunogenic cell death를 조절하기 위한 실험 전략을 평가하는 편리한 workflow를 제공합니다.
서론
Multicellular homeostasis는 잘 조직되고 프로그램된 세포 사멸 메커니즘에 의해 부분적으로 유지됩니다. 이와 같은 프로그램은 일반적으로 “면역관용(tolerogenic)” 또는 “면역원성(immunogenic)” 방식으로 분류됩니다. 면역관용 cell death (면역학적으로 silent apoptosis라고도 함)는 잘 알려진 내인성(intrinsic) 혹은 외인성(extrinsic) 신호 전달 과정을 통해 caspase 활성화와 세포막의 비대칭적 지질 리모델링(lipid remodeling)으로 이어집니다. 중요한 phosphatidylserine의 세포내막에서 외막 표면으로의 translocation 반응은 필수적인 “eat me” 신호를 제공하여 죽어가는 세포가 세포막 완전성(membrane integrity)을 상실하기 전에 식균(phagocytosis)될 수 있도록 합니다. 이러한 형태의 cell death는 염증을 유도하지 않으며 일반적으로 발달 및 조직 리모델링 과정에서 노화, 손상, 중복되거나 필요로 하지 않는 면역 세포 또는 기타 세포 유형을 효율적으로 제거하는 것과 연관됩니다.
Immunogenic cell death로 알려진 염증 반응은 necroptosis, pyroptosis, ferroptosis, NETosis 또는 다른 형태의 apoptosis와 같은 서브루틴으로 추가로 구분될 수 있습니다. DAMPs는 특정한 서브루틴과 무관하게 면역 세포 침윤 및 그로 인한 국소 염증을 지속시키는 세포 밖 환경으로 노출 및/또는 방출됩니다. ICD는 바이러스 및 박테리아의 공격과 종양 특이적 cytotoxic T-cell의 후천적 발달의 중요한 1차 방어선입니다.
Extracellular ATP (eATP)와 high mobility group box B1 (HMGB1) 단백질은 immunogenic cell death 표현형의 확립에 있어 중요한 것으로 알려진 두 가지 DAMPs입니다. 일반적으로 eATP는 보편적인 에너지 전달 분자로 알려져 있지만 다양한 세포 대 세포 신호 전달 반응과 관여하는 것으로 알려져 있습니다. eATP는 다양한 세포 유형에서 발현되는 P2 purinergic receptor를 통해 이와 같은 효과를 매개합니다. ICD의 경우, 죽어가는 세포의 eATP는 수지상 세포 (antigen-processing cells)에 초기 화학유인물질 차이(chemoattractant gradient)를 제공하고, 이후 반응하는 면역 세포에서 paracrine 분비를 통해 염증성 반응을 지속합니다.
HMGB1은 핵에서 구획화된 주요 chromatin 관련 non-histone 단백질입니다. ICD 동안, HMGB1은 세포질로 이동하고 아직 특성이 분석되지 않은 채널 활성 반응 또는 사후 세포막 완전성 손실 후의 수동적 방출을 통해 결국에는 세포 밖 환경으로 방출되게 됩니다. Extracellular HMGB1은 수지상 세포의 성숙과 염증 반응의 전반적인 악화를 촉진하는 다양한 산화환원 상태로 존재합니다.
각 바이오마커 단독으로 immunogenic cell death 반응을 평가하기 위한 예측 값이 있지만, eATP와 HMGB1 두 바이오마커가 같이 존재하는지 여부를 확인하는 것은 단일 매개변수 측정 시보다 표현형에 통계적으로 더 강력한 지수를 제시합니다. 따라서 두 바이오마커를 빠르고 쉽게 측정할 수 있는 것은 ICD 조절에 관련된 발견과 개발 연구의 핵심입니다.
Immunogenic Cell Death (ICD)를 측정하는 기존 방법
eATP와 HMGB1은 ICD 동안 시간이 경과함에 따라 세포 밖 환경으로 방출됩니다. 현재는 일정한 양의 배지를 옮기고 세포 및/또는 세포 debris를 제거하기 위한 저속 원심분리를 실시하여 시간별 세포 상층액 샘플을 반복적으로 샘플링합니다. 이렇게 준비된 상층액은 분석 전까지 일반적으로 +4 또는 -20°C에 보관합니다. 상층액 샘플을 일관성 있게 모으고 처리하지 못하거나, 세포 또는 세포 debris 제거 혹은 샘플을 적절하게 보관하지 못하면 eATP 및 HMGB1 정량이 복잡해질 수 있습니다.
Extracellular ATP는 가장 일반적으로 endpoint 발광 방법을 활용하여 정량하고 있습니다. 이 방법은 과량의 luciferase 효소와 luciferin 기질이 함유된 reaction mixture와 측정하고자 하는 eATP 샘플과의 발광(bioluminescent) 반응에 의해 샘플 eATP에 비례하는 광자(photon)가 생산됩니다. 그러나 상층액의 eATP를 정확하게 측정하는 것은 특히 어려운 과제일 수 있습니다. 예를 들어, 대부분의 형질변환된 세포주는 세포막에 존재하는 ATPase (예: CD39) 발현이 증가되며 높은 ATPase 활성이 유지된 상태로 혈청에서 증식하고 유지됩니다. 이러한 ecto-pyrase 활성은 빠르게 eATP 농도를 급격하게 낮추어 실험 시의 샘플링 및 샘플 처리 과정 중에 eATP를 특히 위험에 빠뜨립니다. (그림 1).
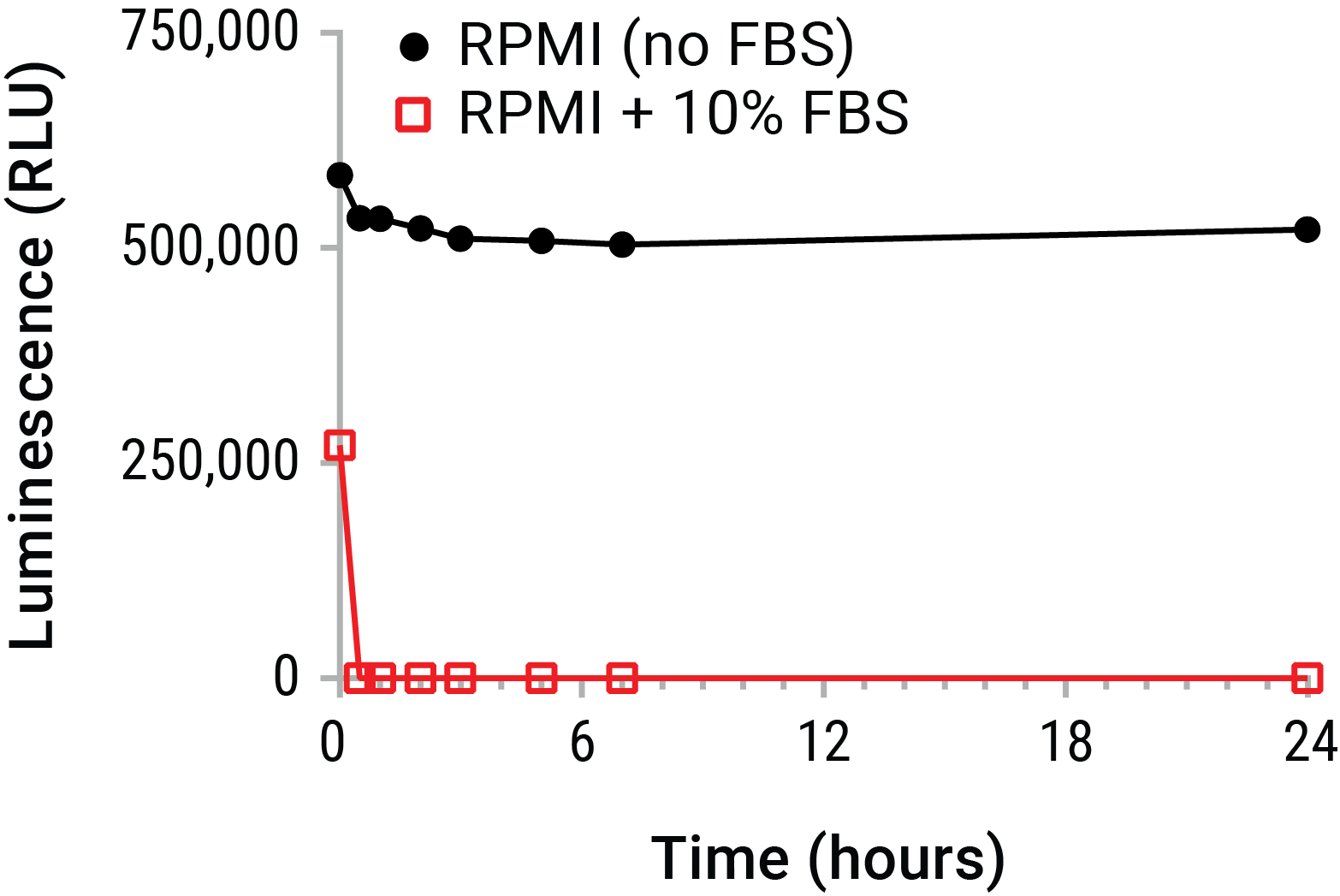
그림 1. Extracellular ATP는 세포 배양 환경에서 불안정함 정제된 ATP (20nM)를 10% FBS 포함된 혹은 포함되지 않은 RPMI 1640 배지에 첨가하였습니다. 샘플은37°C에서 24시간 동안 배양하면서 정해진 시간에 샘플링하였습니다. 시간별 샘플링 완료 후에 CellTiter-Glo® Luminescent Cell Viability Assay를 사용하여 샘플 ATP를 측정하였습니다. 이 결과는 일반적인 상층액 샘플링 방법에 의해 단시간에 높은 eATP 소멸 위험이 있음을 보여줍니다. Assay 전에 이와 같은 ATP 소멸로 인해 eATP 수치가 크게 과소평가될 수 있습니다. 따라서 샘플 내의 ATP 소멸 전 eATP의 실시간 측정이 필요합니다.
HMGB1는 일반적으로 Western blot이나 ELISA로 측정합니다. Western blot이 분석 물질 방출의 핵심적인 생화학적 증거를 제공하지만, 결과가 정량적이지 않고 시간이 오래 걸립니다. ELISA는 시간이 많이 걸리는 힘든 작업이지만 높은 감도를 제공합니다. 하지만 안타깝게도, ELISA 방법은 측정 범위(dynamic range)가 좁다는 단점이 있으며 이러한 제한적인 측정 범위로 인해 분석 전 측정 가능한 선형 범위에서 측정될 수 있도록 샘플을 희석해야 합니다. 샘플 내에 분석 물질의 농도를 알 수 없는 경우, 샘플을 다양한 비율로 희석하여 처리할 샘플의 수가 늘어나게 됩니다. 또한 잘 검증되고 상용화된 assay를 사용하는 데에는 많은 비용이 소모될 수 있습니다.
Extracellular ATP와 HMGB1의 개선된 측정 방법
우리는 샘플링과 샘플 준비 과정이 필요 없는 두 가지 새로운 homogenous assay chemistry를 개발하여 ICD 분석 과정을 크게 간소화하였습니다. 각각의 assay시약을 간단하게 만든 후 이를 각 실험의 샘플 배양 well에 넣어 측정하면 됩니다. RealTime-Glo™ Extracellular ATP Assay시약은 열에 안정적인 Ultra-Glo® luciferase와 화학적으로 순도가 높은 luciferin으로 구성되어 있어 살아있는 세포에 사용이 가능합니다(그림 2). 이러한 구성 성분들을 포함한 배지를 세포에 처리하여 “0” 시간부터 시간에 따른 eATP 방출을 측정하게 됩니다(그림 3). 이러한 반응 물질은 실시간 내성(real-time tolerability)을 고려하여 최적화되었으며, 따라서 아무것도 처리되지 않은 세포의 고유한 생물학적 환경에 영향을 주지 않고, eATP 방출의 기준을 설정할 수 있습니다. 이러한 새로운 방법으로 인해 시간과 노력이 많이 절감된다는 점 이외에도, 실시간 측정을 통해 물질이 처리된 전반적인 시간 동안 eATP 변화를 지속적으로 측정할 수 있습니다. Gas control 또는 CO2-independent배지를 사용한 heated luminometer의 kinetic 모드를 사용한 자동화 format을 통해 최종 노출 시점까지 assay에 “손을 대지 않을” 수 있습니다(그림 4).

그림 2. 발광 기법의 Extracellular ATP detection chemistry

그림 3. RealTime-Glo™ Extracellular ATP Assay 실험 방법
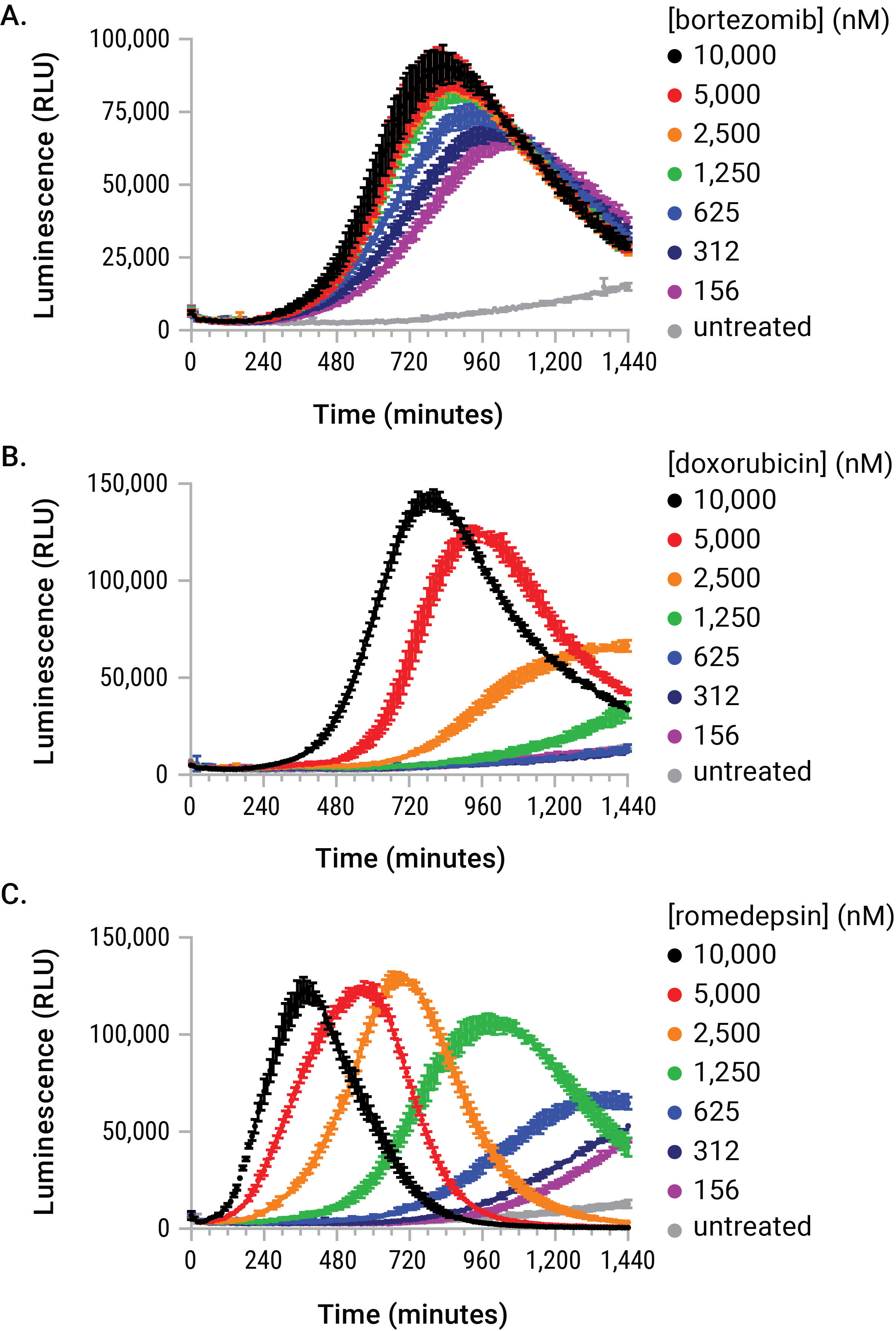
그림 4. 자극에 의해 유도된 eATP 방출은 처리 물질의 농도와 처리 시간에 따라 달라짐 RealTime-Glo™ Extracellular ATP Assay 시약이 포함된 보르테조밉(bortezomib), 독소루비신 (doxorubicin), 로미뎁신(romidepsin)을 U937 cell에 농도별로 처리하였습니다. 물질 처리 시간 동안 생성된 eATP 방출 결과는 처리 농도, 처리 시간, 신호 크기별로 동역학적으로 고유한 결과를 보여줍니다. 이러한 차이로 인해 endpoint eATP 측정 결과는 해석하기 어렵고 부정확할 수 있습니다.
Lumit™ HMGB1 Immunoassay시약은 물질 처리 완료 후 샘플 well에 직접 추가하며 시약에는 luciferase 기질과 luciferase를 생성하는 상보적인(complementary) subunit (LgBiT 혹은 SmBiT)이 라벨된 두 개의 anti-HMGB1 monoclonal 항체가 포함되어 있습니다(그림 5). HMGB1이 샘플 내에 존재하지 않는 경우, 라벨된 anti-HMGB1 항체는 결합하지 못하여 용액 내에 남아있게 되고 이로 인해 약한 발광 값이 만들어집니다. 그리고 HMGB1가 존재하는 경우에는 LgBiT과 SmBiT이 라벨된 두 개의 HMGB1 항체가 HMGB1 epitope에 결합하고 이로 인해 항체에 라벨된 LgBiT와 SmBiT이 가까워 결합하게 됩니다. 이러한 반응의 결과로 샘플 양에 비례적인 발광이 생성됩니다. 따라서 화합물의 ICD 유도 특성은 시간 경과에 따른 반응의 효능과 크기로 설명할 수 있습니다(그림 6). 특히, ICD 유도 방출 반응 후 HMGB1 항원 검출은 Lumit™ 방법을 사용하여 세포 배양 샘플 그대로에서 혹은 배지에서 측정할 수 있습니다. 두 샘플에서 측정한 결과는 기존의 ELISA 방법과 높은 상관관계를 보입니다(그림 7). 또한, 실험에서 얻어진 결과는 제품에 포함된 재조합 human HMGB1을 통한 standard curve와 비교할 수 있습니다. 추가 실험을 통해 HMGB1 mouse isoform과의 높은 교차 반응성(cross-reactivity)이 확인되어 유사한 유도 시스템에서도 분석이 가능합니다.
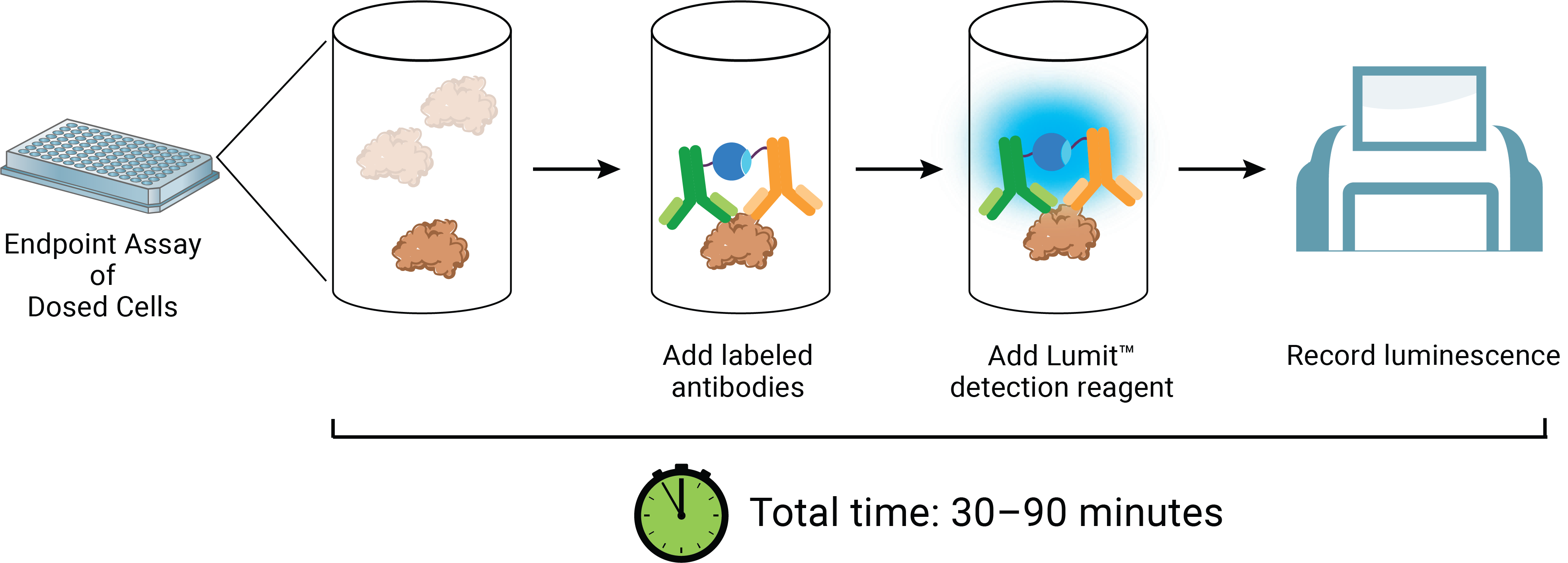
그림 5. Lumit™ HMGB1 Immunoassay concept & workflow
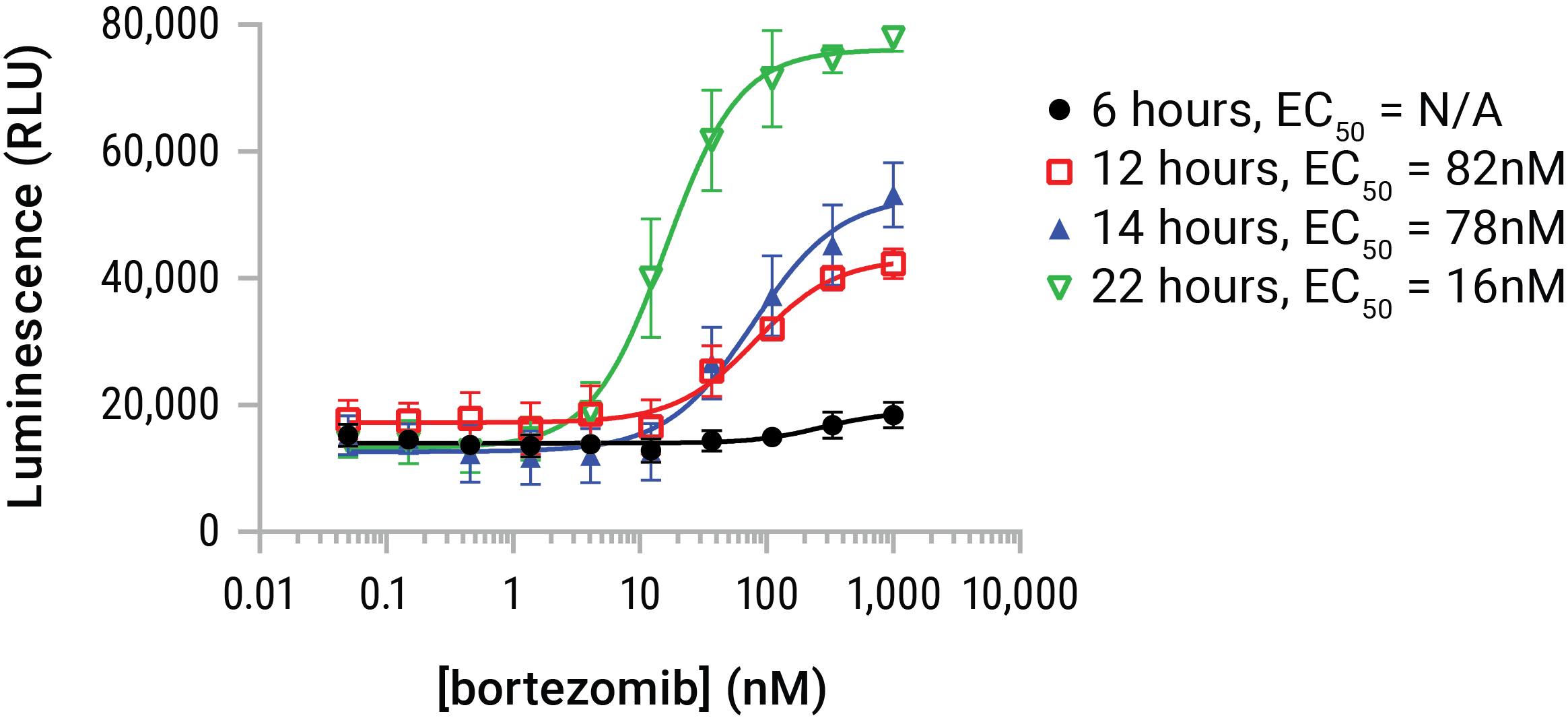
그림 6. HMGB1 방출은 물질 처리 농도와 시간에 따라 달라짐 Serial dilution한 보르테조밉(bortezomib)을 U937 cell에는 일정 시간 (6, 12, 14, 22시간) 동안 처리하였습니다. 반응 후에 Lumit™ HMGB1 Immunoassay 시약을 첨가하고 발광 결과를 측정하였습니다. 보르테조밉(bortezomib)은 약6시간에 HMGB1 방출을 시작하였으며 22시간 동안 추가 방출에 지속적인 영향을 미쳤습니다. 이 모델에서 HMGB1 방출은 시간이 지남에 따라 누적되었지만 HMGB1은 장시간 노출에서 항원성이 손실되는 경향이 있습니다. 따라서 잠재력이나 효능이 알려지지 않은 화합물의 경우 일반적으로 24시간 혹은 48시간 동안 세포에 처리하여 효과에 대한 확인이 필요합니다.
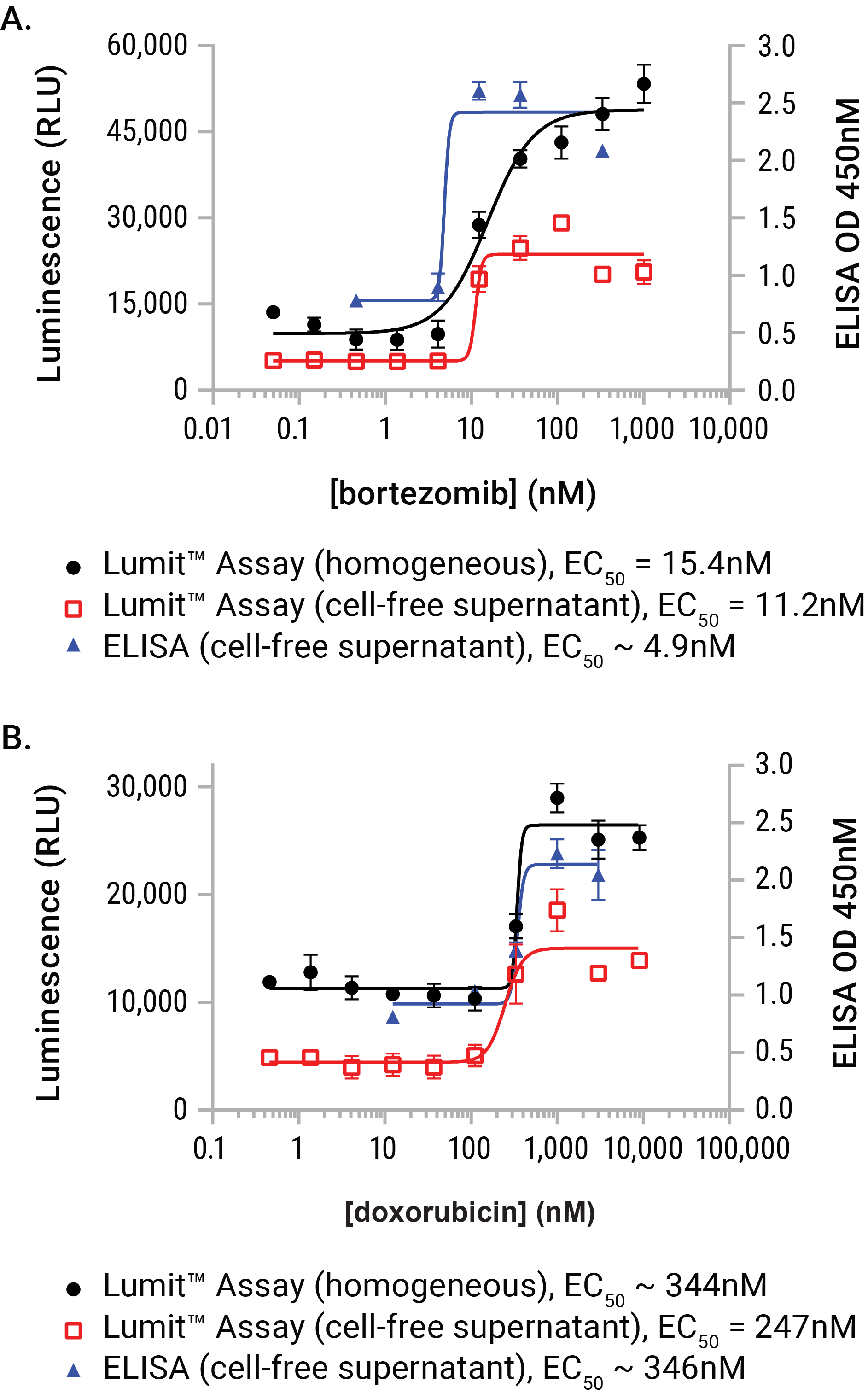
그림 7. Lumit™ HMGB1 Immunoassay와 상용 ELISA 분석 간 성능 비교 보르테조밉(bortezomib) 또는 독소루비신(doxorubicin)를 U937 cell에 24시간 동안 처리하였습니다. 물질 처리 후 동일한 두 개 plate의 parallel well로부터 cell-free 상층액을 준비하였습니다. Lumit™ HMGB1 Immunoassay 시약은 cell이 포함된 plate well과 샘플링한 상층액이 포함된 well에 첨가하였습니다. 또한 상층액 (및 희석한 상층액)은 상용화된 HMGB1 ELISA 제품을 사용하여 분석하였습니다. Lumit 방법으로 두 가지의 샘플에서 분석한 두 결과는 ELISA 결과와 일치함을 보여주었고 결과 측정하는데 휠씬 더 적은 시간이 소요되었습니다. (ELISA 경우 25.5시간 소요된 것과 대조적으로 Lumit™ HMGB1 Immunoassay는 1.5시간 소요됨)
ICD Tool Compound와 세포주 모델을 사용한 Assay 검증
RealTime-Glo® Extracellular ATP Assay와 Lumit™ HMGB1 Immunoassay는 in vitro ICD 발견 및 특성 분석 목적으로 디자인되었습니다. 그래서 다양한 human(그림 8) 및 mouse(그림 9)의 suspension cell line과 attachment-dependent cell line에 DAMP 유도 tool compound를 농도별로 처리하여 assay를 검증하였습니다. ATP 방출 결과는 gas control이 장착된 BMG CLARIOstar™ 또는 CO2 -independent 배지를 사용한 CLARIOstar™를 사용하여 실시간으로 측정하였습니다. Real-time eATP 결과와 Lumit™ HMGB1 결과는 GloMax® Discover를 사용하여 측정하였습니다.

그림 8. Human cell line에서의 dual DAMP 측정 동일한 두 개의 plate에 배양한 U937 세포에 미톡산트론(mitoxantrone)을 serial dilution하여 처리하였습니다. 하나의 plate에는 10% FBS가 포함된 CO2-independent 배지에 RealTime-Glo™ Extracellular ATP Assay 시약을 처리하고GloMax® Discover를 이용한 24시간 동안 발광 결과를 측정하였습니다. 두 번째 plate는 24시간 동안 배양한 후, Lumit™ HMGB1 Immunoassay 시약을 직접 세포 배양 plate에 처리하고 GloMax™ Discover를 사용하여 발광을 측정하였습니다. Top Panels: 미톡산트론(mitoxantrone)에 의해 용량 및 시간에 의존적으로 eATP가 방출되었으며, 이는 시간의 경과에 따라 효능이 점진적 증가하였습니다. Bottom Panels: 재조합 human HMGB1 standard curve에서는 1ng/ml ~ 729ng/ml 농도에서 linearity 가 보여지며 미톡산트론은 eATP와 유사한 dose-dependent HMGB1 방출 반응을 유도하였습니다.

그림 9. Mouse cell line에서의 dual DAMP 측정 EL4 cell을 두 개의 plate에 배양한 후 serial dilution된 이다루비신(idarubicin)을 처리하였습니다. RealTime-Glo™ Extracellular ATP Assay 시약은 10% HS가 포함된 CO2-indenpend 배지에 넣어 plate에 처리하였으며, 발광 값은 GloMax® Discover를 사용하여 24시간 동안 측정하였습니다. 두 번째 plate는 24시간 동안 배양된 후, cell plate에 Lumit™ HMGB1 Immunoassay 시약을 직접 처리하였습니다. 발광 결과는 GloMax™ Discover를 사용하여 측정하였습니다. Top Panels: 이다루비신(idarubicin)에 의해 eATP가 용량 및 시간 의존적으로 방출되었으며, 이는 시간에 따라 효능이 조금 증가하였습니다. Bottom Panels: 재조합 mouse HMGB1 항원 3ng/ml ~ 2,187ng/ml에서 linear curve를 확인하였습니다. 이다루비신은 eATP보다 더 강력한 dose-dependent HMGB1 방출 반응을 유도하였습니다.
요약
Immunogenic cell death 측정을 위한 두 가지 새로운 “homogenous & add-mix-measure” 방식은 새로운 ICD 유도 화합물의 발굴 및 특성 분석 시 많은 양의 화합물 스크링을 가능하게 하며 이에 대한 노력을 줄여줍니다. 이러한 효율성은 불필요한 샘플링과 샘플 준비 과정을 제거하고 실험 방법에서의 incubation과 washing을 제거함으로써 이루어 낸 결과입니다.

