NLRP3 Inflammasome: Flipping the Switch
게시일 : 2021년 07월 28일
선구적인 면역학자이자 생화학자인 Jürg Tschopp 박사가 세상을 떠난 지 10년이 조금 넘었습니다. 그는 2011년 3월 22일 스위스 알프스에서 하이킹 여행 중 비극적으로 사망하였습니다. 사망 당시 Science, Nature 및 Cell을 비롯한 여러 학술지에서 Tschopp 박사가 apoptosis와 면역학 분야에서 이루어 낸 여러 업적을 조명하는 부고 기사를 헌정했습니다.
2002년 스위스 로잔 대학의 Tschopp 박사가 이끄는 연구팀은 전염증성(pro-inflammatory) 사이토카인인 interleukin 1 beta (IL-1β)의 역할을 연구하고 있었습니다. 이 사이토카인은 세포질에서 비활성 전구물질 (pro-IL-1β)로 생성됩니다. 이는 caspase-1에 의해 활성 형태로 cleavage 되지만, caspase-1 자체가 활성화되는 정확한 과정은 당시 알려져 있지 않았습니다. Caspase family member는 caspase recruitment domain 또는 CARD라고 알려져 있는 conserved domain이 포함되어 있으며, 이는 이 도메인이 caspase 활성화에 필수적임을 시사합니다.
연구자들은 caspase-9의 활성화와 연관된 N-terminal CARD motif (Apaf-1)를 포함한 또 다른 단백질과의 유사성을 기반으로 하여, NALP1, NALP2 및 NALP3라 알려져 있는 protein family의 역할을 조사하였습니다. 특히, 이들은 면역 반응에 관여하는 NALP1에 관심을 가졌습니다. Apaf-1와 달리, NALP1는 CARD motif를 C-말단에 포함하고 있지만, N-말단에는 pyrin-like domain (PYD)이라고 알려진 관련 motif가 포함되어 있습니다. 연구팀은 이전에 N-말단의 PYD와 C-말단의 CARD를 포함하는 PYCARD 또는 ASC로 알려진 adapter protein과 NALP1의 PYD 도메인이 상호작용한다는 것을 보여주었습니다.
연구팀의 in vitro binding, 활성화, 면역 검출(immunodetection) 연구 결과는 multi-unit protein complex가 caspase 활성화의 원인이 됨을 보여주었고, 그들은 이러한 complex를 “inflammasome”이라고 명명하였습니다. 이는 caspase-1, caspase-5, PYCARD/ASC 및 NALP1으로 구성되어 있습니다.
구조 및 기능
오늘날, inflammasome은 면역계 연구의 중심 개념이 되었으며 inflammasome 조절 장애는 제2형 당뇨병과 알츠하이머병에 이르는 다양한 질병과 관련이 있습니다. Tschopp 박사가 연구한 NALP protein subfamily는 현재 inflammasome-associated protein인 NLR (nucleotide-binding oligomerization domain (NOD)-like receptor) family의 일부로 알려져 있으며, 지금으로서는 최소 23개의 member가 알려져 있습니다. 그 중 NLRP3와 이에 해당하는 inflammasome이 가장 큰 관심의 대상이 되어왔습니다(참고논문 2에서 리뷰됨).
NLRP3는 3개의 구별된 도메인을 포함하고 있으며 N-말단의 PYD는 ASC의 해당 도메인과 상호작용합니다. 중앙의 NACHT 도메인(3)은 ATP 결합 및 ADP로 전환을 담당하며 단백질의 올리고머화(oligomerization)를 유도합니다. C-말단의 leucine-rich repeat (LRR) 도메인은 기존에는 NLRP3 활성화와 그로 인한 inflammasome assembly에 필수적이라고 생각되었으나, LRR에 대한 역할은 아직까지 논란의 여지가 있습니다(5).
NLRP3 inflammasome의 활성화는 복잡한 과정이지만, 두 가지의 특징적인 단계로 구분해 볼 수 있습니다. 첫 번째는 “프라이밍(priming)” 단계 (Signal 1)로 사이토카인 또는 패턴 인식 수용체(pattern recognition receptor)가 포함된 여러 가지 경로에 의해 시작되며, 그 결과 NLRP3 및 inflammasome 구성요소의 transcriptional activation으로 이어집니다. 두 번째 단계 (활성화 또는 Signal 2)는 RNA 바이러스부터 활성산소종(reactive oxygen species)에 이르는 다양한 PAMP (pathogen-associated molecular patterns)와 DAMP (tissue damage-associated molecular patterns)에 의해 유발됩니다. Inflammasome 구성요소의 transcriptional regulation 및 post-translational modification에 의해 더 복잡하게 조절되나, 최종적으로는 NLRP3 inflammasome assembly가 유도됩니다. 이 protein complex는 caspase-1을 활성화하며, 이후 pro-IL-1β 및 pro-IL-18를 활성 사이토카인으로 전환합니다. Caspase-1 활성화의 또 다른 중요한 결과는 단백질 gasdermin D 단백질의 cleavage를 통해 유도되는 pyroptosis라고 알려진 caspase-dependent apoptosis (programmed cell death)입니다(6). Pyroptosis는 실시간으로 cell death와 함께 caspase-1 활성을 함께 측정하는 multiplexing cell-based assays에 의해 apoptosis와 구분할 수 있습니다(7).
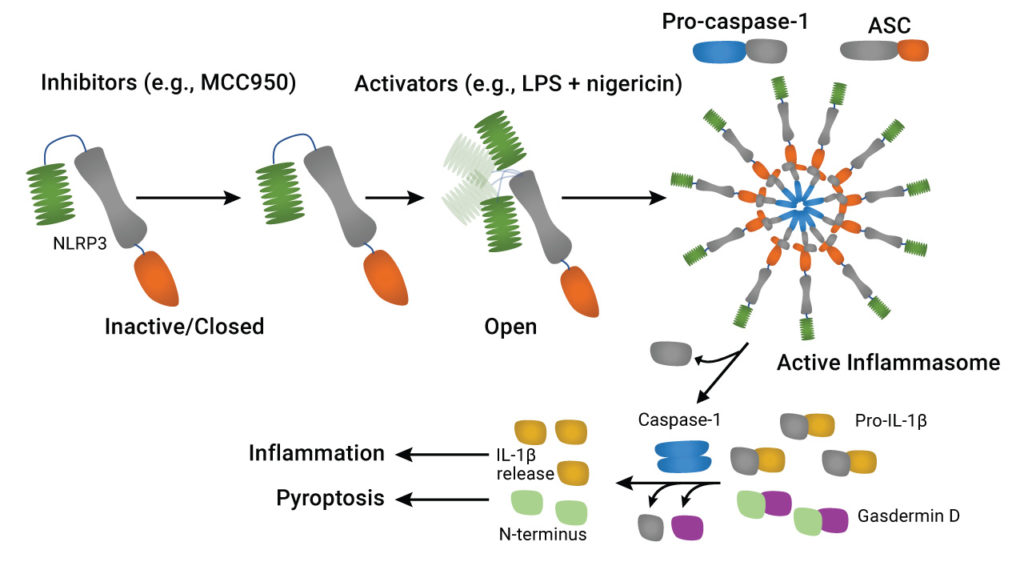
치료 Target
NLRP3 inflammasome 활성화는 다양한 감염성 및 염증성 질환과 관련이 있기 때문에(참고논문 8에서 리뷰됨), 많은 수의 연구가 NLRP3 pathway의 특정 단계를 target으로 하는 치료제 개발에 전념해 왔습니다. 여기에는 다음과 같은 치료제가 포함됩니다(8).
- NACHT 도메인을 target으로 하는 MCC950, MNS 및 OLT1177과 같은 NLRP3 activation inhibitor;
- Caffeic acid phenethyl ester와 같은 ASC inhibitor;
- VX-740 및 VX-765와 같은 caspase-1 inhibitor;
- IL-1β receptor antagonist인 아나킨라(anakinra) 등의 IL-1β inhibitor 및 monoclonal antibody치료제인 카나키누맙(canakinumab)과 게보키주맙(gevokizumab),
- NLRP3 activation pathway의 upstream 및 downstream을 target으로 하는 다양한 간접적인 inhibitor
이와 같은 치료제 중 어느 것도 현재 임상에 적용되고 있지 않지만, 지속적인 신약 개발 과정은 향후 광범위한 염증성 질환에 대한 치료제로 유망합니다. NLRP3 inflammasome 활성화와 관련된 복잡한 pathway를 이해하기 위한 추가적인 연구는 현재까지 개발된 치료제를 개선하고 off-target effect를 최소화하면서 고도로 특이적인 치료제를 개발하는 데 도움이 될 것입니다. 이와 같은 노력을 통해 Tschopp 박사가 20년 전에 “inflammasome”이라는 신조어를 만들었을 때의 비전을 재현할 수 있을 것입니다.
프로메가의 Inflammasome Activation Drug Discovery 페이지에서 inflammasome 활성화에 대해 살펴보세요.
참고문헌
- Martinon, F. et al. (2002) The inflammasome: a molecular platform triggering activation of inflammatory caspases and processing of pro IL-1b. Mol. Cell 10, 417–426.
- Paik, S. et al. (2021) An update on the regulatory mechanisms of NLRP3 inflammasome activation. Cell. Mol. Immunol. 18, 1141–1160.
- Koonin, E.V. and Aravind, L. (2000) The NACHT family – a new group of predicted NTPases implicated in apoptosis and MHC transcription activation. Trends Biochem. Sci. 25, 223–224.
- Broz, P. et al. (2016) Inflammasomes: Mechanism of assembly, regulation and signalling. Nat. Rev. Immunol. 16, 407–420.
- Hafner-Bratkovič, I. et al. (2018) NLRP3 lacking the leucine-rich repeat domain can be fully activated via the canonical inflammasome pathway. Nat. Comm. 9, 5182.
- Bai, B. et al. (2020) NLRP3 inflammasome in endothelial dysfunction. Cell Death Dis. 11, 776.
- O’Brien, M. et al. (2017) A bioluminescent caspase-1 activity assay rapidly monitors inflammasome activation in cells. J. Immunol. Meth. 447, 1–13.
- Seok, J.K. et al. (2021) Therapeutic regulation of the NLRP3 inflammasome in chronic inflammatory diseases. Arch. Pharm. Res. 44, 16–35.