PROTACs: Just the FAQs
게시일 : 2022년 03월 23일

PROTAC은 상류 사회의 칵테일 파티에서 나누는 대화나 글램 매거진의 커버 스토리와 같은 주제는 아니지만, 신약 발굴 업계를 확실히 뒤흔들고 있습니다. PROTAC® degrader는 분자 접착제(molecular glues) 및 LYTACs 등과 같은 관련 화합물과 함께 사용되는 타겟 단백질 degradation 전략을 위한 기본적인 도구입니다. 이 분야의 연구는 빠르게 발전되어 이전에는 "undruggable"로 여겨지던 질환 타겟에 대한 치료법 개발이 가능하게 되었습니다. 본 블로그 포스트에서는 PROTAC과 관련하여 자주 묻는 질문을 요약하여 다룹니다.
PROTAC이란?
PROTAC은 PROteolysis-TArgeting Chimera의 약어입니다. 이름에서 알 수 있듯이, 이 분자는 여러 기능적 unit을 포함하며 세포의 쓰레기 처리 시스템인 ubiquitin-proteasome system (UPS)이 degradation 반응을 일으키도록 세포 내의 특정 단백질을 타겟팅하는 데 사용됩니다. 일반적인 PROTAC은 linker로 분리된 두 개의 기능적 단백질 결합 단위 또는 ligand로 구성됩니다.
PROTAC은 어떻게 작용하나요?
PROTAC의 이중기능적 속성은 세포 내의 작용 방식에 있어 매우 중요합니다. PROTAC의 ligand 중 하나 ("warhead"라고도 불림)는 타겟 관심 단백질에 결합합니다. 다른 ligand ("anchor")는 UPS machinery의 component (일반적으로 E3 ubiquitin ligase를 모집하는 단백질)에 결합합니다. 그리고 이 두 단백질이 PROTAC에 동시에 결합되면 ternary complex가 형성됩니다. 이렇게 형성된 complex에 의해, E3 ligase는 타겟 단백질에 ubiquitin을 순차적으로 추가되도록 하며 이렇게 생성된 ubiquitin chain이 UPS를 끌어당겨, 결과적으로 타겟 단백질이 degradation되게 됩니다.
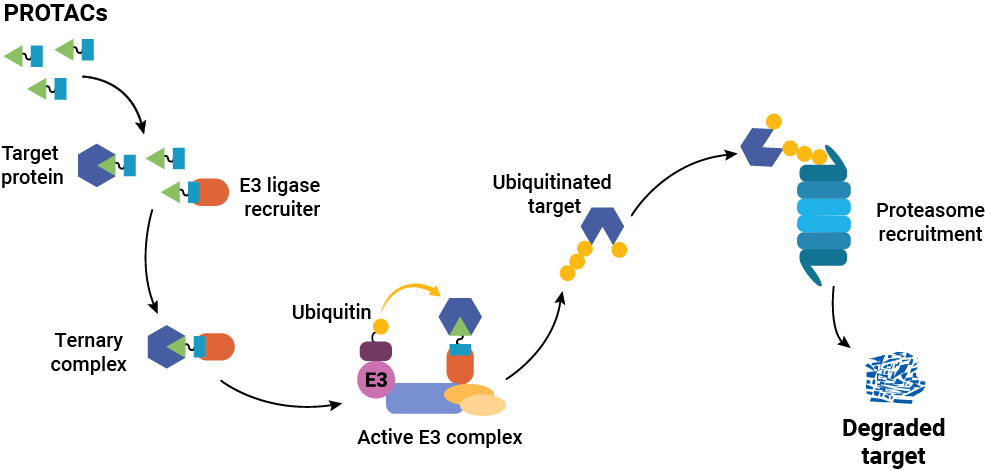
An overview of the mechanism of action for a typical PROTAC.
PROTAC은 타겟 단백질의 ubiquitination 후에 complex로부터 방출되므로 이 과정에서 기본적으로 재활용됩니다. 따라서 상대적으로 적은 양의 PROTAC은 많은 양의 타겟 단백질 degradation을 유도할 수 있습니다.
PROTAC이 왜 중요한가요?
타겟 단백질이 질환과 관련된 것으로 확인되면, 기존의 신약 개발 전략에서는 해당 단백질에 대한 inhibitor를 찾는 데 중점을 두었습니다. 대부분의 경우, 이와 같은 접근법은 small molecule이 타겟 단백질의 활성 부위에 결합하여 그 활성을 조절하는 것을 확인하기 위해 약물 후보 물질 라이브러리를 스크리닝합니다. 이러한 "occupancy-driven pharmacology" 접근법은 특히 효소 활성이 없는 단백질의 경우 한계가 있습니다 (1). 결과적으로, 알려진 단백질 타겟의 약 85%는 여전히 undruggable 타겟으로 남아 있습니다 (2). 또한 적절한 inhibitor가 존재하는 경우에도 치료 효과를 얻기 위해서는 이러한 약물을 고농도로 사용해야 하는 경우가 많습니다 (3).
PROTAC은 inhibitor 기반의 약물 개발 접근 방식의 단점을 극복합니다. 이는 대부분의 단백질 타겟의 여러 부위에 결합하도록 설계할 수 있으며, 촉매 작용 메커니즘을 통해 타겟 단백질 양을 가역적이고 농도 의존적으로 조절할 수 있습니다. 일부 상황에서, 특히 복잡한 신호전달 경로를 연구할 때 타겟 단백질을 degradation하는 것이 단순히 해당 타겟 단백질의 활성을 억제하는 것보다 유리할 수 있습니다.
어떻게 PROTAC이 발견되었나요?
첫 번째로 보고된 PROTAC은 2001년 Craig Crews와 Raymond Deshaies의 연구실에서 합성되어 테스트한 펩타이드입니다 (4). 이 proof-of-concept 연구에서 PROTAC은 methionine aminopepitidase-2 (MetAP-2)를 ubiquitin ligase complex의 component로 타겟팅하도록 설계되었습니다. 이 연구에서 PROTAC 농도에 비례적으로 Met-AP2가 ubiquitination 되고 degradation 됨을 밝힘으로써, 이후 PROTAC 발전의 발판을 마련하였습니다. 펩타이드 기반의 PROTAC 적용이 추가적으로 시도되었으나, 분자의 낮은 세포 투과성(cell permeability)으로 인해 적용에 어려움이 있었습니다 (reviewed in 5). Small molecule PROTAC을 성공적으로 적용한 최초의 연구는 2008년에 발표되었습니다 (6). 이 분자는 높은 세포 투과성을 가지며, PROTAC 농도에 비례적으로 안드로겐 수용체(androgen receptor)를 성공적으로 타겟팅하여 degradation 반응을 일으켰습니다. 이는 안드로겐 수용체 발현이 증가하는 것이 특징인 전립선암에 적용할 수 있음을 시사합니다. 이와 같은 초기 발견 이후 PROTAC 연구는 기하급수적인 성장을 하였습니다 (reviewed in 7). 현재 PROTAC 개발은 small molecule 신약 개발에 있어 기존의 inhibitor 기반의 접근 방법에 대한 흥미로운 대안을 제공합니다. PROTAC 개발을 추적하는 웹 액세스 데이터베이스인 PROTAC-DB에 따르면 2021년 4월 현재 2,258개의 PROTAC이 개발 중입니다.
어떻게 효과적인 PROTAC을 설계할 수 있나요?
PROTAC을 합리적으로 설계하기 위해서는 여러 가지 요소를 고려해야 합니다. 구조 연구는 결정학적 데이터(crystallographic data)에서 관심 타겟의 결합 부위에 대한 통찰력을 제공할 수 있지만, 이러한 데이터는 다수의 타겟이나 잠재적 PROTAC에 사용할 수는 없습니다. 따라서 타겟 단백질 degradation 과정의 각 단계에서의 기작을 연구함으로써 합리적으로 PROTAC을 설계할 수 있습니다. Paiva와 Crews는 PROTAC 설계와 관련된 일반적인 고려 사항에 대한 리뷰 논문을 발표했으며 (8), Leissing 연구팀은 ternary complex 형성에 중점을 두고 구조 기반 설계 원리에 대한 개요를 발표했습니다 (9). 또 다른 리뷰 논문에서는 다양한 유형의 암과 관련된 chromatin remodeling complex의 component를 타겟 하는 structure-guided PROTAC 설계에 대해 논의했습니다 (10). 일반적으로 PROTAC 디자인은 PROTAC의 component인 타겟 결합 ligand (또는 "warhead"), linker, E3 ligase-recruiting ligand (또는 “anchor”)에 초점을 맞춥니다.
Target-Binding Ligand
대부분의 경우 PROTAC warhead는 타겟 단백질에 대한 높은 affinity를 갖습니다. 설계 전략으로 많은 특성 분석이 수행되었으며 타겟 단백질에 특이적으로 결합하는 것으로 알려진 small molecule inhibitor를 활용할 수 있습니다. 그러나 여러 타겟에 결합하는 ligand는 이점이 없으며, 타겟 단백질에 대한 affinity가 약한 ligand라 하더라도 ternary complex 형성 시 안정적인 경우라면 타겟 degradation을 효율적으로 유도할 수 있습니다 (11). PROTAC 개발에서 발견된 흥미로운 부분은 trivalent PROTAC를 사용하는 것입니다 (12). 이 분자에는 타겟 단백질에 결합하는 두 개의 ligand가 포함되어 있으며 타겟에 대한 결합력(avidity) 증가로 인해 ternary complex의 안정성이 더욱 높아지고 타겟 degradation이 증가합니다.
Linker
PROTAC linker는 설계 단계에서 종종 간과되는 경우가 있어, 그 중요성이 과소평가될 수 있습니다. 더 복잡하고 기능적인 linker를 많이 사용하게 되면, ternary complex가 안정화되고 전반적인 degradation 효율이 개선되는 장점이 있습니다 (reviewed in 13). Linker 조성과 길이, 둘 다 PROTAC 효율성의 최적화에 있어 중요한 역할을 합니다 (14).
E3 Ligand
600개 이상의 E3 ubiquitin ligase가 존재하는 것으로 알려져 있지만, 대부분의 E3 ligase-recruiting ligand는 이 효소 중 일부만을 타겟으로 하여 개발되고 있습니다 (15). 이 중 가장 흔한 것은 von Hippel-Lindau (VHL) E3 ligase와 cereblon (CRBN)입니다. 철저한 문헌 검토를 통해 E3 ligase에 결합하는 ligand를 설계할 때 사용할 수 있는 합성 경로에 대한 인사이트를 얻을 수 있습니다 (15). 이 리뷰 논문에서는 적합한 ligand 선택하는데 도움이 되는 tool과 E3 ligand 개발 시에 많이 사용되는 상용화된 building block 리스트를 제공합니다.
PROTAC이 어떻게 작용하는지 살아있는 세포에서 확인할 수 있나요?
타겟 단백질 degradation 과정의 각 단계를 확인하기 위한 다양한 생화학적 assay가 있지만, 기존의 방법으로는 일반적으로 end-point 결과만을 얻을 수 있으며 high-throughput analysis에는 적합하지 않습니다. 실시간으로 degradation을 모니터링할 수 있는 Live-cell assay를 사용하면, 상당한 이점을 얻을 수 있습니다 (16). 이와 같은 assay 중 NanoBRET™-based 방법은, 높은 감도로 편리하게 PROTAC kinetics를 측정할 수 있을 뿐 아니라 살아있는 세포에서의 복잡한 degradation 과정에 대한 폭넓은 이해를 제공합니다 (17). NanoBRET™ VHL and CRBN Ternary Complex Starter Kits은 ternary complex 형성을 측정하는 동시에 타겟 단백질의 degradation을 정량 분석할 수 있는 편리한 방법을 제공합니다.
PROTAC은 clinical application에 사용되고 있나요?
2019년 임상 시험에 들어간 첫 번째 PROTAC은 Arvinas, Inc.가 전립선암 치료를 위해 개발한 약물입니다. 이 회사는 2022년 2월 PROTAC, ARV-110 또는 bavdegalutamide가 "전이성 거세저항성 전립선암(metastatic castration-resistant prostate cancer, mCRPC)에서 anti-tumor 활성 및 환자 이익의 근거를 지속적으로 제공한다"는 중간 결과 보고서를 발표했습니다. Arvinas는 Pfizer와의 협력을 통해 또 다른 PROTAC인 ARV-471을 유방암 치료에 사용한 긍정적인 초기 치료 결과를 보고했습니다. PROTAC 및 관련 degrader의 타겟이 되는 다른 종류의 암도 있습니다 (reviewed in 18, 19). 전임상 연구에서 유망한 발전은 지금까지 효과적으로 타겟팅하기 어려웠던 KRAS-driven cancer을 타겟으로 PROTAC을 사용하는 것입니다 (20).
PROTAC 신약 개발에 관심이 있지만 어떻게 시작해야 하는지 모르시나요? Promega의 Compound Profiling Services가 도와드릴 수 있습니다.
더 알고 싶으신가요? 타겟 단백질 degradation 관련 포스트를 Promega Connections에서 확인해 보세요.
PROTAC은 Arvinas Operations, Inc.의 등록 상표입니다.
참고문헌
- Valeur, E. and Jimonet, P. (2018) New modalities, technologies, and partnerships in probe and lead generation: enabling a mode-of-action centric paradigm. J. Med. Chem. 61, 9004–9029.
- Pathmanathan, S. et al. (2022) Drugging the undruggable proteins in cancer: A systems biology approach. Curr. Opin. Chem. Biol. 66, 102079.
- Adjei, A.A. (2006) What is the right dose? The elusive optimal biologic dose in phase I clinical trials. J. Clin. Oncol. 24, 4054–4055.
- Sakamoto, K.M. et al. (2001) Protacs: Chimeric molecules that target proteins to the Skp1–Cullin–F box complex for ubiquitination and degradation. Proc. Natl. Acad. Sci. USA 98(15), 8554–8559.
- Pettersson, M. and Crews, C. (2019) PROteolysis TArgeting Chimeras (PROTACs)—Past, present and future. Drug Discov. Today Technol. 31, 15–27.
- Schneekloth, A.R. et al. (2008) Targeted intracellular protein degradation induced by a small molecule: En route to chemical proteomics. Bioorganic Med. Chem. Lett. 18, 5904–5908.
- Békés, M. et al. (2022) PROTAC targeted protein degraders: the past is prologue. Nat. Rev. Drug Discov. 21,181–200.
- Paiva, S.-L. and Crews, C. (2019) Targeted protein degradation: elements of PROTAC design. Curr. Opin. Chem. Biol. 50, 111–119.
- Leissing, T.M. et al. (2020) Structure driven compound optimization in targeted protein degradation. Drug Discov. Today Technol. 37, 73–82.
- Farnaby, W. et al. (2019) BAF complex vulnerabilities in cancer demonstrated via structure-based PROTAC design. Nat. Chem. Biol. 15, 672–680.
- Bondeson, D.P. et al. (2018) Lessons in PROTAC design from selective degradation with a promiscuous warhead. Cell Chem. Biol. 25, 78–87.
- Imaide, S. et al. (2021) Trivalent PROTACs enhance protein degradation via combined avidity and cooperativity. Nat. Chem. Biol. 17, 1157–1167.
- Troup, R.I. et al. (2020) Current strategies for the design of PROTAC linkers: a critical review. Explor. Target Antitumor Ther. 1, 273–312.
- Zagidullin, A. et al. (2020) Novel approaches for the rational design of PROTAC linkers. Explor. Target Antitumor Ther. 1, 381–390.
- Bricelj, A. et al. (2021) E3 ligase ligands in successful PROTACs: an overview of syntheses and linker attachment points. Front. Chem. 9, 707317.
- Daniels, D.L. et al. (2019) Monitoring and deciphering protein degradation pathways inside cells. Drug Discov. Today Technol. 31, 61–68.
- Riching, K.M. et al. (2018) Quantitative live-cell kinetic degradation and mechanistic profiling of PROTAC mode of action. ACS Chem. Biol. 13, 2758−2770.
- Mullard, A. (2021) Targeted protein degraders crowd into the clinic. Nat. Rev. Drug Disc. 20, 247–250.
- Qi, S.-M. et al. (2021) PROTAC: an effective targeted protein degradation strategy for cancer therapy. Front. Pharmacol. 12, 692574.
- Zhou, C. et al. (2022) Discovery of the first-in-class agonist-based SOS1 PROTACs effective in human cancer cells harboring various KRAS mutations. J. Med. Chem. 65, 3923−3942.